设NA表示阿伏加德罗常数的数值,则下列说法正确的是
| A.标准状况下,4.48 L水中含有的分子数目为0.2NA |
| B.0.1 mol钠与足量水反应转移的电子数目为0.1NA |
| C.0.2 mol·L-1CuSO4溶液中含有的SO42-离子数目为0.2NA |
| D.0.5molKClO3中含有Cl-的数目为0.5 NA |
某密闭容器中发生如下反应:X(g) + 3Y(g) 2Z(g)ΔH < 0。下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。
2Z(g)ΔH < 0。下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。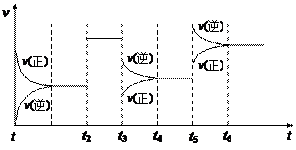
下列说法中正确的是:()
| A.t2时加入了催化剂 |
| B.t3时降低了温度 |
| C.t5时增大了压强 |
| D.该反应最初是从逆反应开始的 |
对于可逆反应:2A(g)+B(g) 2C(g)△H<0,下列图象正确的是
2C(g)△H<0,下列图象正确的是 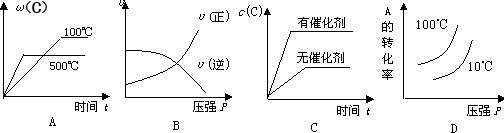
镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O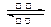 Cd(OH)2 + 2Ni(OH)2。有关该电池的说法正确的是:()
Cd(OH)2 + 2Ni(OH)2。有关该电池的说法正确的是:()
| A.充电时阳极反应:Ni(OH)2-e- + OH- ="=" NiOOH + H2O |
| B.充电过程是化学能转化为电能的过程 |
| C.放电时负极附近溶液的碱性不变 |
| D.放电时电解质溶液中的OH -向正极移动 |
一定条件下,对于可逆反应X(g)+3Y(g) 2Z(g),若X、Y、Z的起始浓度分别为c
2Z(g),若X、Y、Z的起始浓度分别为c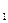 、c
、c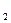 、c
、c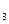 (均不为零),到达平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08 mol/L,则下列判断正确的是:()
(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08 mol/L,则下列判断正确的是:()
A.c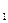 :c :c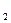 ="1:2" ="1:2" |
B.平衡时,Y和Z的生成速率之比为2:3 |
| C.X、Y的转化率相等 | D.c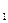 的取值范围为0.04 mol/L<c 的取值范围为0.04 mol/L<c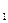 <0.14 mol/L <0.14 mol/L |
把下列4种X溶液,分别加入4个盛有10mL2mol·L-1盐酸的烧杯中,均加水稀释到50mL,此时X和盐酸缓慢地进行反应,若不考虑液体混合后体积的微小变化,其中反应速率最大的是()
| A.20mL3mol·L-1的X溶液 | B.20mL 2mol·L-1的X溶液 2mol·L-1的X溶液 |
| C.10mL4mol·L-1的X溶液 | D.10mL2mol·L-1的X溶液 |