某温度下,在固定容积的密闭容器中,可逆反应A(g)+3B(g) 2C(g)达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1。保持温度不变,以2∶2∶1的物质的量之比再充入A、B、C,则
2C(g)达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1。保持温度不变,以2∶2∶1的物质的量之比再充入A、B、C,则
A.平衡不移动
B.再达平衡时,n(A)∶n(B)∶n(C)仍为2∶2∶1
C.再达平衡时,C的体积分数增大
D.再达平衡时,正反应速率增大,逆反应速率减小
向0.1mol/L的NaOH溶液中慢慢滴加同浓度的醋酸溶液,离子浓度之间的关系不可能出
现的是
| A.c(CH3COO-)>c(H+) = c(Na+)>c(OH-) | B.c(Na+)>c(OH-) >c(CH3COO-)>c(H+) |
| C.c(OH-)>c(Na+)>c(H+)>c(CH3COO-) | D.c(Na+) >c(CH3COO-)>c(OH-) >c(H+) |
两体积相同的密闭容器中均充入1 mol X和1mol Y,分别于300℃和500℃开始发生反应:X(g)+Y(g)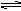 3Z(g)。Z的含量(Z%)随时间t的变化如下图所示。已知在t3时刻改变了某一实验条件。相关判断正确的是
3Z(g)。Z的含量(Z%)随时间t的变化如下图所示。已知在t3时刻改变了某一实验条件。相关判断正确的是
| A.曲线a是500℃时的图像 | B.正反应是吸热反应 |
| C.t3时刻可能是降低了温度 | D.t3时刻可能是增大了压强 |
几种短周期主族元素的结构与性质信息如下表:
| 元素编号 |
元素性质或原子结构 |
| T |
原子最外层共有6种不同运动状态的电子 |
| X |
氢化物水溶液呈碱性 |
| Y |
短周期中原子半径最大 |
| Z |
元素最高正价是+3价其最高价氧化物可做耐火材料 |
符合题意的判断是
A.X的气态氢化物一定比T的气态氢化物稳定
B.Y单质与T单质不可直接按原子个数1:1化合
C.常温下Z单质能溶于X最高价氧化物对应水化物的浓溶液中
D.一定条件下元素T或X的氢化物可分别与其氧化物反应生成T或X单质
正确的实验操作是实验成功的基本保证。下列实验操作正确的是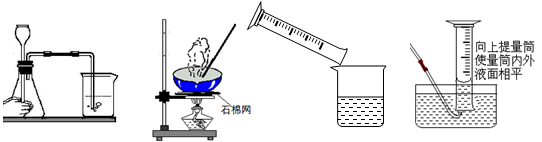
| A.检查装置气密性 | B.蒸发 | C.转移液体 | D.读取气体体积 |
每年由于腐蚀造成的钢铁损失约占年产量的10~20%,金属的防腐十分重要。钢铁防腐方法有许多种,图—1与图—2是两个典型的例子。对其中原理的描述正确的是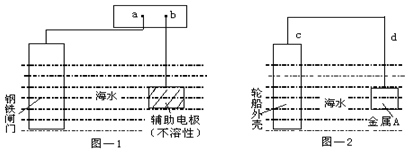
| A.图—1:a为电源正极 | B.图—1:辅助电极上的反应:O2+4e+2H2O→4OH- |
| C.图—2:电子流动方向d→c | D.图—2:金属A可以是耐腐蚀的金属铜 |