NA为阿伏伽德罗常数,下列叙述正确的是
| A.18gH2O中含有的质子数为NA |
| B.常温常压下,Na2O2与足量H2O反应,每生成1 molO2,转移电子的数目为4NA |
| C.46gNO2和N2O4混合气体中含有原子总数为3NA |
| D.物质的量浓度为0.5 mol·L-1的MgCl2的溶液中,含有Cl-个数为NA |
在工业生产硫酸中,吸收塔内用来吸收三氧化硫的物质是
| A.H2O | B.稀H2SO4 | C.浓H2SO4 | D.NH3·H2O |
有三组物质:① NO2和溴蒸气;②乙醛、苯、硝基苯三种无色液体;③ CaC2、CuSO4(无水)、CaCO3、Na2SO4、干燥的碱石灰(加有少量酚酞)五种固体,只要有水就能区别开的是()
| A.① | B.①③ | C.②③ | D.①②③ |
验证乙酸乙酯密度,溶解性和水解三项性质的合理实验是()
| A.将其滴入水中,随即滴加碱液并迅速加热至沸腾 |
| B.将其滴入沸腾的碱液中观察 |
| C.将其滴入水中观察片刻,再滴加含有酚酞的碱液并缓缓加热 |
| D.将其滴入沸腾的水中观察 |
某化学课外小组欲用固体与液体反应(不需加热),快速简便制取一满瓶(125mL)干燥的氧气。
(1)从A~G中所提供的仪器(或装置),选出所需要的(填序号);除导管及胶管外,还需要的仪器用品有。选用的试剂为。
(2)用上述所选的气体发生装置,除可制取O2、H2、CO2外,请写出还可用此装置制取的两种其它气体与制取该气体所需的试剂。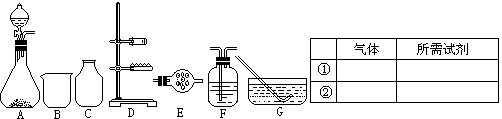
下列实验操作,正确的是()
①中和滴定时,用标准液润洗滴定管,用待测液润洗移液管和锥形瓶,并在锥形瓶内滴入l mL指示剂
②配制物质的量溶液时,将称量好的溶质溶于盛有适量水的烧杯中,待溶解后立即倾入容量瓶中,继续进行洗涤和定容
③用NaOH溶液和可溶性铝盐溶液大量制取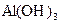
④制取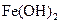 时,吸取NaOH溶液的胶头滴管的末端应插入
时,吸取NaOH溶液的胶头滴管的末端应插入 溶液中,再逐渐注入NaOH溶液
溶液中,再逐渐注入NaOH溶液
⑤蔗糖加稀硫酸水解后,将水解液滴入银氨溶液,水浴加热后即可见银镜
| A.①②③ | B.②⑤ | C.④ | D.以上都不正确 |