下列陈述I、II均正确且有因果关系的是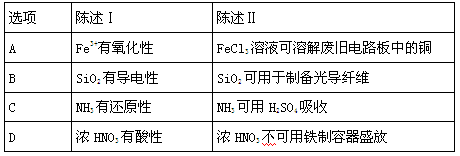
下列说法正确的是()
| A.钠保存在煤油里的原因之一是它极易与氧气反应 |
| B.铜在空气中很容易燃烧 |
| C.铝表面的氧化膜疏松,不能保护内层金属 |
| D.铁锈的主要成分是Fe3O4 |
在无色透明的溶液中可以大量共存的离子组是()
| A.OH- K+ Al3+ | B.OH- NH4+ Cl- |
| C.Cu2+ NO3- Cl- | D.Mg2+ K+ Cl- |
欲配制浓度为1.00mol/L的氯化钠溶液100mL,用不到的仪器是()
| A.100mL容量瓶 | B.分液漏斗 | C.玻璃棒 | D.烧杯 |
下列实验操作或装置正确的是()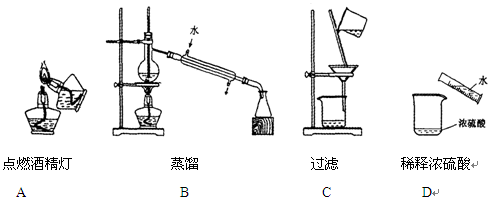
下列反应属于氧化还原反应的是()
A.H2SO4+2NaOH  Na2SO4+2H2O Na2SO4+2H2O |
B.2NaHCO3  Na2CO3 + CO2↑ + H2O Na2CO3 + CO2↑ + H2O |
C.NH3 + HCl  NH4Cl NH4Cl |
D.CuO + H2 Cu + H2O Cu + H2O |