已知X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素。其中只有Z是金属,W的质子数是Y的2倍,X、Y、W在周期表中的相对位置关系如下图。下列说法正确的是 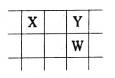
| A.五种元素中原子半径最大的是X,离子半径最大的是Q离子 |
| B.五种元素中Q的最高价氧化物所对应的水化物的酸性最强 |
| C.Y与Z形成的化合物一定是碱性氧化物 |
| D.Z与Q形成的化合物水溶液一定显酸性 |
下列对沉淀溶解平衡的描述正确的是( )
| A.反应开始时,溶液中各离子浓度相等 |
| B.沉淀溶解达到平衡时,沉淀的速率和溶解的速率相等 |
| C.沉淀溶解达到平衡时,溶液中溶质的离子浓度相等,且保持不变 |
| D.沉淀溶解达到平衡时,如果再加入难溶性的该沉淀物,将促进溶解 |
根据Ksp值比较下列几种难溶物溶解度最小的是()
| A.BaSO4 | B.CaCO3 | C.AgCl | D.AgI |
CuS沉淀可溶于()
| A.热浓硝酸 | B.浓氨水 | C.盐酸 | D.醋酸 |
1L Ag2C2O4饱和溶液中质量为0.06257g,若不考虑离子强度,水解等因素,Ag2C2O4的Ksp是()
| A.4.24×10-8 | B.3.50×10-11 | C.2.36×10-10 | D.8.74×10-12 |
向饱和BaSO4溶液中加水,下列叙述正确的是
| A.BaSO4的溶解度不变,Ksp不变 | B.BaSO4的溶解度减小,Ksp增大 |
| C.BaSO4的溶解度不变,Ksp增大 | D.BaSO4的溶解度增大,Ksp不变 |