下图是“空气中氧气体积分数测定”实验的改进装置。主要操作是:在实际容积为150mL的集气瓶里,先装进50mL的水,再按图连好仪器,按下热的玻璃棒,白磷立即被点燃。(白磷40℃即燃烧,燃烧产物与红磷相同)
(1)该实验中白磷需稍过量,目的是 。
(2)白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是 ;若实验成功,最终集气瓶中水的体积约为 mL。
(3)该实验可推论出氮气_________(填“易”或“难”)溶于水和其化学性质________(填“活泼”或“不活泼”)的结论。
(4)若将白磷换成炭粉,该实验能否获得成功?为什么?_____成功,原因________________________________________________________。
(5)集气瓶里预先装进的50mL水,在实验过程中起到哪些作用? (填写序号)
A.加快集气瓶内气体冷却 B.液封导气管末端以防气体逸出 C.吸收五氧化二磷
下表列出了1 cm3活性炭在常温常压下所能吸附的常见气体的体积,试分析活性炭吸附气体的难易跟气体的哪些性质有关。 
在天平两端各放等质量的两个锥形瓶(瓶口用单孔塞和导管连接起来,气球中装有等质量的大理石),如图所示。左盘锥形瓶中盛有M克水,右盘锥形瓶中盛有M 克稀盐酸,天平平衡。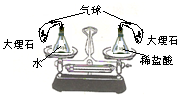
(1)实验开始时,将气球中的大理石倒入锥形瓶中,
观察到的现象是,天平的指针(填“偏左”、 “偏右”或“在标尺中央”,下同)。
(2)待上述实验的反应完成后,将锥形瓶瓶口上的单孔塞、导管和气球去掉,天平的指针;原因是。
(提示:大理石与水不反应,与盐酸反应的化学方程式为:CaCO3 + 2HCl =CaCl2 + H2O + CO2↑)
在点燃条件下,A和B反应生成C和D。反应前后分子种类的变化微观示意图如下: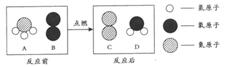
请回答:
(1)一个B分子中含有个原子。
(2)A中氮元素和氢元素的质量比。
(3)4种物质中属于化合物的是(填图中字母)。
(4)该反应中,生成C和D的质量比为(结果用最简整数比表示)。
现有下图所示的实验装置,请回答问题: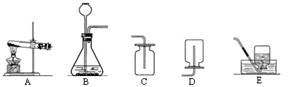
(1)在加入药品之前应对实验装置进行。
(2)用高锰酸钾制氧气可选用的发生装置是(填字母序号,下同);用过氧化氢制氧气可选用的发生装置是。你认为两套装置不一样的主要原因是。
(3)某同学用E装置收集氧气,理由是,为什么导管口刚有气泡冒出时,不宜立即收集。
(4)若选用B装置制备气体时应注意什么。
青篙素(化学式为 C15H22O5)是治疗疟疾的特效药,28.2g 青篙素中含碳元素的质量为。