配制100mL、1.0mol·L-1的NaOH溶液,下列情况会导致溶液浓度偏高的是
| A.读数时,俯视确定凹液面与刻度线相切 |
| B.容量瓶使用前经蒸馏水清洗后还残留有少量蒸馏水 |
| C.定容后把容量瓶颠倒摇匀,发现液面低于刻度线,又补足了所缺的水 |
| D.配制过程中,用蒸馏水洗涤烧杯和玻璃棒后,未把洗涤液移入容量瓶 |
莽草酸的结构简式如图,下列关于莽草酸的说法不正确的是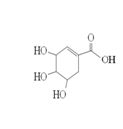
| A.相同条件下等物质的量的莽草酸和正戊醛(C5H10O)完全燃烧时的耗氧量相同 |
| B.分子中含有两种含氧官能团,可发生取代反应 |
| C.1mol莽草酸既可与2mol氢气发生加成反应,也可与4molNaOH发生中和反应 |
| D.可用溴水鉴别莽草酸、乙醇、四氯化碳和苯 |
有机化学在日常生活应用广泛,下列有关说法不正确的是
| A.相同条件下,正丁烷、新戊烷、异戊烷的沸点依次增大 |
| B.苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色 |
| C.甲苯和Cl2光照下的反应与乙醇和乙酸的反应属于同一类型的反应 |
| D.有芳香气味的C9H18O2在酸性条件下加热可水解产生相对分子质量相同的两种有机物,则符合此条件的C9H18O2的结构有16种 |
一定条件下存在反应:C(s)+H2O(g) CO(g)+H2(g)△H>0。向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。
CO(g)+H2(g)△H>0。向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。
| 容器 |
甲 |
乙 |
丙 |
| 容积 |
0.5 L |
0.5 L |
V |
| 温度 |
T1 ℃ |
T2 ℃ |
T1 ℃ |
| 起始量 |
2 molC 1 molH2O |
1 molCO 1 molH2 |
4 molC 2 molH2O |
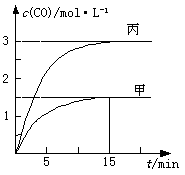
下列说法正确的是
A.甲容器中,反应在前15 min的平均速率v(H2)="0.1" mol·L-1·min-1
B.丙容器的体积V<0.5 L
C.当温度为T1 ℃时,反应的平衡常数K=2.25
D.乙容器中,若平衡时n(H2O)="0.4" mol,则T1< T2
25℃时,下列各溶液中有关微粒的物质的量浓度关系正确的是
| A.在0.1 mol·L-1Na2S溶液中:2c(Na+) =c(S2-)+c(HS-) +c(H2S) |
| B.pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合:c(Na+)+ c(H+)= c(OH-)+c(CH3COO-) |
| C.向0.1 mol·L-1盐酸与0.1 mol·L-1K2CO3溶液等体积混合: c(K+) >c(Cl-)>c(HCO3-)>c(OH-)>c(H+) |
| D.向0.1 mol·L-1NH4HSO4溶液中滴加NaOH至溶液恰好呈中性: |
c(Na+)>c(NH4+)>c(SO42-)>c(OH-) =c(H+)
下列依据相关实验得出的结论正确的是
| A.加入硫酸铜可使锌与稀硫酸的反应速率加快,说明Cu2+具有催化作用 |
| B.纤维素的水解产物能够发生银镜反应,说明纤维素是一种还原性糖 |
| C.向某溶液中滴加硝酸酸化的Ba(NO3)2溶液产生白色沉淀,说明该溶液中含有SO42- |
| D.等物质的量浓度的H3PO4溶液的pH比H2SO4溶液大,说明硫比磷的非金属性强 |