有A、B、C、D、E五块金属片,进行如下实验:①A、B用导线相连后,同时浸入稀硫酸溶液中,A为负极;②C、D用导线相连后,同时浸入稀硫酸溶液中,电流由D→导线→C;③A、C相连后,同时浸入稀硫酸溶液中,C极产生大量气泡;④B、D用导线相连后,同时浸入稀硫酸溶液中,D极发生氧化反应;⑤用惰性电极电解含B离子和E离子的溶液,E先析出。据此,判断五种金属的活动性顺序是
A.A>B>C>D>E B.A>C>D>B>E
C.C>A>B>D>E D.B>D>C>A>E
碱性硼化钒(VB2)—空气电池工作时反应为:4VB2 + 11O2 = 4B2O3 + 2V2O5。用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是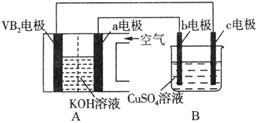
| A.电解过程中,c电极表面先有红色物质析出,后有气泡产生 |
| B.外电路中电子由c电极流向VB2电极 |
| C.VB2电极发生的电极反应为: 2VB2 + 11H2O - 22e- = V2O5 + 2B2O3 + 22H+ |
| D.若B装置内的液体体积为100 mL,则CuSO4溶液的物质的量浓度为0.05 mol/L |
某小组为研究电化学原理,设计甲、乙、丙三种装置(C1、C2、C3均为石墨)。下列叙述正确的是
| A.甲、丙中是化学能转变为电能,乙中是电能转变为化学能 |
| B.C1、C2分别是阳极、阴极,锌片、铁片上都发生氧化反应 |
| C.C1上和C3上放出的气体相同,铜片上和铁片上放出的气体也相同 |
| D.甲中溶液的pH逐渐升高,丙中溶液的pH逐渐减小 |
下列溶液中的离子一定能大量共存的是
| A.在加入铝粉能产生氢气的溶液中:NH4+、Fe2+、SO42-、NO3- |
| B.室温下由水电离出的氢离子浓度c(H+)=1×10-14mol/L的溶液中:Ba2+、NO3-、K+、ClO- |
| C.能使酚酞变红色的溶液中:Na+、K+、AlO2-、CO32- |
| D.在c(HCO3-)="0.1" mol·L-1的溶液中:NH4+、AlO2-、Cl-、NO3- |
常温下,下列溶液中各离子浓度关系正确的是
| A.醋酸溶液与NaOH溶液相混合后,所得溶液呈中性:c(Na+)>c(CH3COO—) |
| B.浓度为0.1 mol·L-1的碳酸钠溶液:c(Na+)=2c(CO32—)+c(HCO3—) +c(H2CO3) |
| C.pH=12的氨水溶液与pH=2的盐酸等体积混合:c(Cl—)>c(NH4+)>c(H+)>c(OH—) |
| D.等物质的量的氨水和盐酸混合后的溶液:c(H+)=c(OH-)+c(NH3·H2O) |
把4mol A和2.5mol B混合于2L密闭容器中,发生反应:3A(g)+2B(s)  xC(g)+D(g),5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.05mol•L-1•min-1,下列结论错误的是
xC(g)+D(g),5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.05mol•L-1•min-1,下列结论错误的是
| A.A的平均反应速率为0.15 mol•L-1•min-1 |
| B.平衡时,C的浓度为0.25mol•L-1 |
| C.B的平均反应速率为0.1 mol•L-1•min-1 |
| D.平衡时,容器内压强为原来的0.875倍 |