某温度时,浓度都是1mol/L的两种气体X2和Y2,在密闭容器中发生可逆反应生成气体Z,充分反应后X2的浓度为0.4mol/L,Y2的浓度为0.8mol/L,生成的Z的浓度为0.4mol/L,则该反应的化学方程式(Z用X、Y表示)是
A.X2+2Y2 2XY2 2XY2 |
B.2X2+Y2 2X2Y 2X2Y |
C.X2+3Y2 2XY3 2XY3 |
D.3X2+Y2 2X3Y 2X3Y |
一定温度下,下列溶液的离子浓度关系式正确的是
| A.pH=5的H2S溶液中,c(H+)=c(HS)=1×10-5mol·L-1 |
| B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 |
| C.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH-)+c(HC2O4-) |
| D.pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③ |
用FeCl3溶液腐蚀印刷电路板上的铜,所得溶液中加入铁粉。对加入铁粉充分反应后的溶液分析合理的是
| A.若无固体等剩余,则溶液中一定有Fe3+ |
| B.若有固体存在,则溶液中一定有Fe2+ |
| C.若溶液中有Cu2+,则一定没有固体析出 |
| D.若溶液中有Fe2+,则一定有Cu析出 |
将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与所通入CO2的体积关系如图所示.下列关于整个反应过程中的叙述不正确的是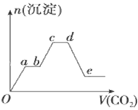
| A.Oa段反应的化学方程式是Ba(OH)2+CO2═BaCO3↓+H2O |
| B.ab段与cd段所发生的反应相同 |
| C.de段沉淀减少是由于BaCO3固体消失 |
| D.bc段反应的离子方程式是2AlO2﹣+3H2O+CO2═2Al(OH)3↓+CO32﹣ |
下列离子方程式与所述事实相符且正确的是
| A.在强碱性溶液中,次氯酸钠将Mn2+氧化成MnO2:Mn2++ClO-+H2O=MnO2↓+Cl-+2H+ |
| B.用稀硝酸清洗做过银镜反应的试管:Ag+NO3-+4H+=Ag++NO↑+2H2O |
| C.向FeBr2溶液中通入过量的Cl2:2Fe2++2Br-+2Cl2==2Fe3++Br2+4Cl- |
D.用铁棒作阴极、炭棒作阳极电解饱和氯化钠溶液: 2Cl-+2H2O H2↑+Cl2↑+2OH - H2↑+Cl2↑+2OH - |
混合下列各组物质使之充分反应,加热蒸干产物并高温下灼烧至质量不变,最终残留固体为纯净物的是
| A.向CuSO4溶液中加入适量铁粉 |
| B.等物质的量浓度、等体积的FeCl3与KI溶液混合 |
| C.等物质的量的NaHCO3与Na2O2溶于水 |
| D.在Na2SiO3溶液中通入过量CO2气体 |