C、N、S都是重要的非金属元素。下列说法正确的是
A.三者对应的氧化物均为酸性氧化物
B.三者的单质直接与氧气反应都能至少生成两种氧化物
C.相同温度下,等物质的量浓度的Na2CO3、NaNO3、Na2SO3溶液的pH大小顺序:NaNO3<Na2SO3<Na2CO3
D.CO2、NO2、SO2都能与H2O反应,其反应原理相同
已知X、Y、Z、E、F五种常见物质含有同一元素M,在一定条件下它们有如下转化关系,Z是NO,下列推断不合理的是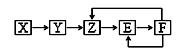
| A.X可能是一种氢化物 |
| B.若Y为单质,Y生成Z属于化合反应 |
| C.E可能是一种有色气体 |
| D.F中M元素的化合价可能为+5 |
下列说法正确的是
| A.0.01 mol·L-1氨水与0.01 mol·L-1盐酸等体积混合,所得溶液中c(H+)=c(OH-) |
| B.氯水中离子浓度大小关系是:c(H+)>c(Cl-)>c(OH-)>c(ClO-) |
| C.25℃时,将pH=a的醋酸溶液稀释10倍后,溶液的pH=b,则a>b |
D.25℃时,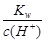 =0.1 mol·L-1的溶液中,Na+、CO32-、Cl-一定能大量共存 =0.1 mol·L-1的溶液中,Na+、CO32-、Cl-一定能大量共存 |
在密闭容器中进行反应CH4(g)+H2O(g) CO(g)+3H2(g) ΔH>0 , 测得c(CH4)随反应时间(t)的变化如图所示。下列判断正确的是
CO(g)+3H2(g) ΔH>0 , 测得c(CH4)随反应时间(t)的变化如图所示。下列判断正确的是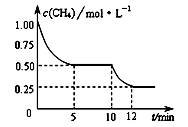
| A.0~5 min内, v(H2)=0.1 mol·(L·min)-1 |
| B.反应进行到12min时,CH4的转化率为25% |
| C.恒温下,缩小容器体积,平衡后H2浓度减小 |
| D.10 min时,改变的外界条件可能是升高温度 |
用右图所示装置(必要时可加热试管),不能完成的实验是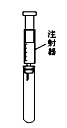
| A.试管中盛酚酞试液,验证氨气的水溶液呈碱性 |
| B.试管中盛酸性高锰酸钾溶液,探究SO2的还原性 |
| C.试管中盛稀氢氧化钠溶液, 验证CO2与NaOH反应的产物 |
| D.装置中充满NO2气体,探究压强对化学平衡的影响 |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.22.4 L CO2与CO的混合气体中含碳原子数为NA |
| B.常温下,1L 0.1 mol·L-1的NH4NO3溶液中氮原子数为0.2 NA |
| C.在反应KIO3 + 6HI=KI + 3I2 + 3H2O中,每生成3 mol I2转移的电子数为6 NA |
| D.在铁参与的反应中,5.6 g铁完全反应失去的电子数一定为0.3 NA |