实验表明:将氯水滴加到一张蓝色石蕊试纸上,试纸上会出现如图所示的半径慢慢扩大的内外两个圆环,且两环颜色不同,
下列有关说法中不正确的是
| A.此实验表明氯水具有酸性、漂白性 |
| B.内环呈白色外环呈红色或浅红色 |
| C.内外环上颜色的差异表明此变化过程中,中和反应比氧化还原反应快 |
| D.氯水中形成次氯酸的反应中还原产物是HClO |
已知0.02 mol·L-1CH3COOH溶液和0.01 mol·L-1NaOH溶液以等体积混和后溶液呈酸性,则该混合液中微粒浓度关系正确的
| A.c(CH3COO-)>c(Na+) |
| B.c(Na+) +c(H+) =c(OH-) +c(CH3COOH)+c(CH3COO-) |
| C.c(CH3COOH)>c(CH3COO-) |
| D.c(CH3COOH)+c(CH3COO-)="0.02" mol·L-1 |
将足量的BaCO3粉末分别加入下列溶液中,充分溶解至溶液饱和。各溶液中Ba2+的浓度最小的为
| A.10 mL 0.2 mol/LNa2CO3溶液 | B.40 mL水 |
| C.50 mL 0.01 mol/L 氯化钡溶液 | D.100 mL 0.01 mol/L盐酸 |
在a、b两个相同的容器中,分别加入相同量的A和B,发生可逆反应:A(g)+3B(g)  2C(g)(正反应为放热反应),两容器中C的体积分数与时间的关系如图所示,则a、b两线不同的可能原因是
2C(g)(正反应为放热反应),两容器中C的体积分数与时间的关系如图所示,则a、b两线不同的可能原因是
| A.a的温度高于b |
| B.a使用了催化剂,而b未用 |
| C.a的压强大于b |
| D.a的温度低于b |
可逆反应4NH3(g)+5O2(g)  4NO(g)+6H2O(g),若反应速率分别用
4NO(g)+6H2O(g),若反应速率分别用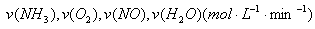 表示,则关系正确的是
表示,则关系正确的是
已知空气—锌电池的电极反应为:锌片:Zn + 2OH――2e-=" ZnO" + H2O石墨:1/2O2+H2O + 2e- = 2OH-据此判断,锌片是:
| A.负极,并被氧化 | B.负极,并被还原 |
| C.正极,并被氧化 | D.正极,并被还原 |