下列离子方程式与所述事实相符且正确的是
| A.氯气与水反应:Cl2+H2O=2H++Cl-+ClO- |
B.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-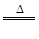 Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
| C.用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O |
| D.Fe3O4与稀HNO3反应:Fe3O4+8H+ =Fe2++2Fe3++4H2O |
一定条件下硝酸铵受热分解的化学方程式为:5NH4NO3=2HNO3+4N2+9H2O,在反应中被氧化与被还原的氮原子数之比为
| A.5∶3 | B.5∶4 | C.1∶1 | D.3∶5 |
根据转化关系判断下列说法正确的是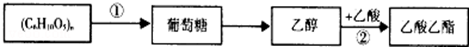
| A.(C6H10O5)n可以是淀粉或纤维素,二者均属于多糖,互为同分异构体 |
| B.可以利用银镜反应证明反应①的最终产物为葡萄糖 |
| C.酸性高锰酸钾可将乙醇氧化为乙酸,将烧黑的铜丝趁热插乙醇中也可得到乙酸 |
| D.在反应②得到的混合物中倒入饱和氢氧化钠溶液并分液可得到纯净的乙酸乙酯 |
下列反应属于取代反应的组合是
①CH3CH=CH2+Br2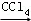 CH3CHBrCH2Br
CH3CHBrCH2Br
②CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
③2CH3CH2OH+O2 2CH3CHO+2H2O
2CH3CHO+2H2O
④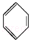 +Br2
+Br2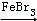
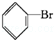 +HBr.
+HBr.
| A.①② | B.③④ | C.①③ | D.②④ |
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电.其电池反应为:2CH3OH+3O2+4OH﹣ 2CO32﹣+6H2O,则下列说法错误的是()
2CO32﹣+6H2O,则下列说法错误的是()
| A.放电时CH3OH参与反应的电极为正极 |
| B.充电时电解质溶液的pH逐渐增大 |
| C.放电时负极的电极反应为:CH3OH﹣6e﹣+8OH﹣=CO32﹣+6H2O |
| D.充电时每生成1molCH3OH转移6mol电子 |
应用元素周期律分析下列推断,其中正确的组合是
①碱金属单质的熔点随原子序数的增大而降低
②Cs是第ⅠA族元素,Cs失电子能力比Na的强
③砹(At)是第VIIA族,其氢化物的稳定性大于HCl
④第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
⑤第三周期金属元素的最高价氧化物对应水化物,其碱性随原子序数的增大而减弱.
| A.①③⑤ | B.①②⑤ | C.②③⑤ | D.①②④ |