高铁酸钠(Na2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强、无二次污染的绿色水处理剂。工业制高铁酸钠的方法有如下两种:
湿法制备的主要离子反应为:2Fe(OH)3 +3ClO-+4OH- = 2FeO42-+3Cl-+5H2O ,
干法制备的主要反应方程为:2FeSO4 +6Na2O2 = 2Na2FeO4 +2Na2O +2Na2SO4 +O2↑
则下列有关说法不正确的是
| A.高铁酸钠中铁显+6价 |
| B.湿法中FeO42—是氧化产物 |
| C.干法中每生成1mol Na2FeO4转移4mol电子 |
| D.K2FeO4可氧化水中的H2S、NH3,生成的Fe(OH)3胶体还能吸附悬浮杂质 |
已知NaCN溶液呈碱性,(CN)2与卤素单质的性质相似,CN-的还原性介于Br-、I-之间。下列变化不能发生的是( )
A.HCN H++CN- H++CN- |
| B.(CN)2+CH2=CH2―→NC—CH2—CH2—CN |
| C.(CN)2+2Br-=2CN-+Br2 |
| D.(CN)2+2OH-=CN-+CNO-+H2O |
金属钛(Ti)性能优越,被称为继铁、铝后的“第三金属”。工业上以金红石为原料制取Ti的反应为
aTiO2+bCl2+cC aTiCl4+cCO反应(1)
aTiCl4+cCO反应(1)
TiCl4+2Mg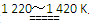 Ti+2MgCl2反应(2)
Ti+2MgCl2反应(2)
关于反应(1)、(2)的分析不正确的是( )
①TiCl4在反应(1)中是还原产物,在反应(2)中是氧化剂;
②C、Mg在反应中均为还原剂,被还原;
③在反应(1)、(2)中的还原性C>TiCl4,Mg>Ti;
④a=1,b=c=2;
⑤每生成19.2 g Ti(Mr=48),反应(1)、(2)中共转移4.8 mol e-。
A.①②④ B.②③④ C.③④ D.②⑤
a mol FeS与b mol Fe3O4投入到V L c mol·L-1的硝酸溶液中恰好完全反应,假设只产生NO气体。所得澄清溶液的成分是Fe(NO3)3和H2SO4的混合液,则反应中未被还原的硝酸为( )
| A.(a+3b) mol | B.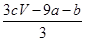 mol mol |
C. mol mol |
D.(cV-3a-9b) mol |
ClO2是一种杀菌消毒效率高的水处理剂,实验室可通过以下反应制得:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法中不正确的是( )
| A.ClO2是还原产物 |
| B.1 mol KClO3参加反应,失去电子为1 mol |
| C.H2C2O4在反应中被氧化 |
| D.H2C2O4的还原性大于ClO2的还原性 |
事实上,许多氧化物在一定条件下能与Na2O2反应,且反应极有规律,如Na2O2+SO2=Na2SO4,2Na2O2+2SO3=2Na2SO4+O2,据此你认为下列反应方程式中不正确的是( )
| A.Na2O2+N2O3=NaNO2+NaNO3 |
| B.Na2O2+2NO2=2NaNO2+O2 |
| C.Na2O2+N2O4=2NaNO3 |
| D.2Na2O2+2Mn2O7=4NaMnO4+O2 |