下列离子方程式表达正确的是
A.向漂白粉溶液中通入少量CO2的离子方程式: 2ClO-+CO2+H2O===2HClO+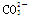 |
B.用铜为电极电解饱和食盐水:2Cl-+2H2O Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
| C.50 mL 1mol/L的NaOH溶液中通入0.03 mol H2S:5OH-+3H2S=HS-+2S2-+5H2O |
| D.碳酸氢镁溶液中加入过量石灰水:Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+MgCO3↓+2H2O |
下列说法正确的是
| A.图I所示装置用于Cu和浓H2SO4制取少量的SO2气体 |
| B.图Ⅱ装置可验证非金属性:Cl>C>Si |
| C.图Ⅲ可用于收集气体H2、CO2、Cl2、NH3 |
| D.图Ⅳ表示将SO2气体通入溴水中,所得溶液的pH变化 |
下列离子组中所给离子在水溶液中能大量共存,且当加入试剂后反应的离子方程式书写完全且正确的是
| 选项 |
离子组 |
加入试剂 |
发生反应的离子方程式 |
| A |
Fe3+、S2ˉ、Clˉ、Na+ |
NaOH溶液 |
Fe3++3OHˉ=Fe(OH)3↓ |
| B |
Na+、Al3+、Clˉ、SO42ˉ |
少量KOH溶液 |
Al3++3OHˉ=Al(OH)3↓ |
| C |
H+、Fe2+、SO42ˉ、NO3ˉ |
BaCl 2溶液 |
SO42ˉ+Ba2+=BaSO4↓ |
| D |
Na+、K+、ClOˉ、SO42ˉ |
通入少量SO2 |
2ClOˉ+SO2+H2O=2HClO+SO32ˉ |
0.6mol/L的Fe2(SO4)3和1.2mol/L的CuSO4的混合溶液200mL,加入一定量铁粉充分反应后,测得溶液中Fe2+与Cu2+物质的量之比为2:1,则加入铁粉的物质的量为
| A.0.16 mol | B.0.22mol | C.0.30mol | D.0.48mol |
一定条件下,中学化学常见物质甲、乙之间存在如下转化关系,Z是
| A.HCl | B.FeCl2 | C.KOH | D.NaHCO3 |
利用右图所示装置进行下列实验,能得出相应实验结论的是
| 选项 |
① |
② |
③ |
实验结论 |
 |
| A |
浓盐酸 |
MnO2 |
NaOH |
制氯气并吸收尾气 |
|
| B |
浓硫酸 |
蔗糖 |
溴水 |
浓硫酸具有脱水性、氧化性 |
|
| C |
稀盐酸 |
Na2SO3 |
Ba(NO3)2溶液 |
SO2与可溶性钡盐均可生成白色沉淀 |
|
| D |
浓硝酸 |
Na2CO3 |
Na2SiO3溶液 |
酸性:硝酸>碳酸>硅酸 |