将等物质的量浓度的CuSO4溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图,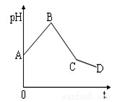
则下列说法正确的是
| A.阳极产物一定是Cl2,阴极产物一定是Cu |
| B.BC段表示在阴极上是H+放电产生了H2 |
| C.整个过程中阳极先产生Cl2,后产生O2 |
| D.CD段表示阳极上OH一放电破坏了水的电离平衡,产生了H+ |
有关下图所示原电池(盐桥中装有含琼脂的KCl饱和溶液)的叙述,正确的是
| A.铜是阳极,铜片上有气泡产生。 |
| B.铜离子在铜片表面被还原。 |
| C.电流从锌片经导线流向铜片。 |
| D.反应中,盐桥中的K+会移向ZnSO4溶液。 |
下列有关金属腐蚀及其防护的叙述 中不正确的是
| A.金属的电化学腐蚀比化学腐蚀更普遍 |
| B.用牺牲锌块的方法来保护船身 |
| C.用铜质铆钉铆接铁板,铁板不易被腐蚀 |
| D.浸泡在水中钢闸门,水面附近区域的腐蚀程度大于长期在水下的部分 |
有A、B、C、D四种金属。将A与B用导线连接起来,浸入电解质溶液中,B不易腐蚀。将A、D分别投入等浓度盐酸中,D比A反应剧烈。将铜浸入B的盐溶液里,无明显变化。如果把铜浸入C的盐溶液里,有金属C析出。据此判断它们的活动性由强到弱的顺序是
A.D>C>A>B
B.D>A>B>C
C.D>B>A>C
D.B>A>D>C
某分子的球棍模型如下图所示。已知该分子中所有原子的最外层均达到8电子稳定结构,原子间以单键相连。下列有关说法中错误的是
| A.X原子可能为第ⅤA族元素 |
| B.Y原子为第ⅠA族元素 |
| C.该分子中既含有极性共价键又含有非极性共价键 |
| D.从圆球的大小分析,该分子可能为N2F4 |
下列有关化学键和化合物的说法不正确的是
| A.离子键就是阴阳离子间强烈的静电作用 |
| B.H和Cl形成的分子中存在的是极性共价键 |
| C.氯化铵中没有金属元素,所以不是离子化合物 |
| D.11号与9号元素能够形成离子化合物,该化合物中存在离子键 |