用于金属焊接的某种焊条,其药皮由大理石、水泥、硅铁等配制而成。下列说法不正确的是
| A.生产水泥的原料是大理石、纯碱、石英,其组成一般为Na2O·CaO·6SiO2 |
B.Si与NaOH溶液反应的离子方程式为:Si+2OH-+H2O= +2H2↑ +2H2↑ |
| C.焊接过程中,药皮在高温下产生了熔渣和使金属不被氧化的气体,该气体是CO2 |
| D.经处理后的熔渣36.0g(仅含Fe2O3、Al2O3、SiO2),加入足量稀盐酸,分离得到11.0 g固体;滤液中加入过量NaOH溶液,分离得到21.4g固体;则此熔渣中Al2O3的质量分数为25% |
下列说法正确的是
| A.某气体能使澄清石灰水变浑浊,则该气体是CO2 |
| B.向某溶液中加入AgNO3溶液,产生白色沉淀,则原溶液中有Cl- |
| C.向某溶液中加入Ba(NO3)2溶液,产生白色沉淀,加入稀硝酸沉淀不溶解,则原溶液中有SO |
| D.向某溶液中加入NaOH并加热,产生可使湿润的红色石蕊试纸变蓝的气体,则原溶液中有NH |
运用盖斯定律可方便地计算出难以通过实验直接测定的反应热。已知:P4(白磷,s)+5O2(g)=P4O10(s) ΔH=-2983.2kJ·mol-1,P(红磷,s)+ O2(g)=
O2(g)= P4O10(s) ΔH=-738.5kJ·mol-1,则白磷转化为红磷的热化学方程式为
P4O10(s) ΔH=-738.5kJ·mol-1,则白磷转化为红磷的热化学方程式为
| A.P4(白磷,s)=4P(红磷,s) △H=-29.2kJ·mol-1 |
| B.P4(白磷,s)=4P(红磷,s) △H=+29.2kJ·mol-1 |
| C.P4(白磷,s)=4P(红磷,s) △H=-2244.7kJ·mol-1 |
| D.P4(白磷,s)=4P(红磷,s) △H=+2244.7kJ·mol-1 |
在催化剂、400℃时可实现氯的循环利用,如图是其能量关系图,下列分析正确的是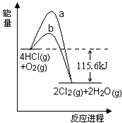
| A.曲线a是使用了催化剂的能量变化曲线 |
| B.反应物的总键能高于生成物的总键能 |
| C.反应的热化学方程式为: 4HCl(g)+O2(g)  2Cl2+2H2O(g)﹣115.6 kJ 2Cl2+2H2O(g)﹣115.6 kJ |
| D.若反应生成2mol液态水,放出的热量高于115.6kJ |
在密闭容器中发生可逆反应4NH3+5O2 4NO+6H2O(g),以下是不同情况下的反应速率,其中最快的是
4NO+6H2O(g),以下是不同情况下的反应速率,其中最快的是
| A.v(O2)=0.001mol/(L·S) |
| B.v(NH3)="0.002" mol/(L·S) |
| C.v(H2O)="0.003" mol/(L·h) |
| D.v(NO)="0.008" mol/(L·S) |
下列关于金属腐蚀的叙述不正确的是
| A.黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| B.与生铁相比纯铁更容易被腐蚀 |
| C.金属的吸氧腐蚀和析氢腐蚀都属于电化学腐蚀 |
| D.金属腐蚀的本质是M - ne‑ = Mn+ |