可逆反应a A(s)+b B(g) c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是
c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是
| A.达平衡后,加入催化剂则C%增大 |
| B.达平衡后,若升温,平衡左移 |
| C.化学方程式中b >c +d |
| D.达平衡后,增加A的量有利于平衡向右移动 |
下列叙述正确的是( )
A.人造象牙的主要成分结构简式为 ,是通过加聚反应制得的,其单体是HCHO ,是通过加聚反应制得的,其单体是HCHO |
B.高分子 的单体是 的单体是 |
C. 经过处理可直接从线型结构变为体型结构 经过处理可直接从线型结构变为体型结构 |
D. 经过处理,不能直接由线型结构变成体型结构 经过处理,不能直接由线型结构变成体型结构 |
下列对一些塑料制品的叙述中,不正确的是( )
| A.塑料凉鞋可以热修补,是因为制作材料是线型高分子材料,具有热塑性 |
| B.聚乙烯塑料是线型高分子材料,具有热塑性,可反复加工多次使用 |
| C.塑料制品废弃后采用深埋作业,是因为塑料制品易分解 |
| D.酚醛塑料制品如电木插座不能进行热修补,是因为酚醛塑料是体型分子,不具有热塑性 |
下列高分子化合物中,可以溶解在有机溶剂中的是( )
| A.废轮胎上刮下的橡胶粉末 |
| B.纤维素 |
| C.酚醛塑料 |
| D.聚乙烯 |
复合材料是由两种或多种性质不同的材料通过物理和化学复合,组成具有两个或两个以上相态结构的材料,该类材料的性能优于组成中的任意一种单独材料,下面对于复合材料的描述错误的是( )
| A.复合材料的使用可以使导弹的射程有很大的提高 |
| B.复合材料可能具有组分单独不具有的独特性能 |
| C.复合材料会对环境造成污染 |
| D.复合材料具有强度大的特点 |
工业上生产“的确良”通常以乙二醇、对苯二甲酸为原料合成,反应式为:nHOCH2CH2OH+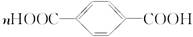
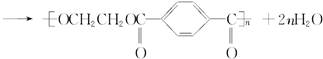 合成时,若消耗乙二醇的物质的量比对苯二甲酸多0.5%,上述聚合物的链节数n为( )
合成时,若消耗乙二醇的物质的量比对苯二甲酸多0.5%,上述聚合物的链节数n为( )
| A.100 | B.200 | C.300 | D.400 |