下列溶液与100mL0.5mol/LNa2SO4溶液中的 Na+的物质的量浓度相等的是
| A.200mL0.5mol/LNaCl溶液 | B.100mL1mol/LNa2CO3溶液 |
| C.100mL0.5mol/LNa3PO4溶液 | D.1L1mol/LNaOH溶液 |
元素的原子结构决定其性质和在周期表中的位置。下列说法正确的是:
| A.元素原子的最外层电子数等于元素的最高化合价 |
| B.多电子原子中,在离核较近的区域内运动的电子能量较高 |
| C.P、S、Cl得电子能力和最高价氧化物对应的水化物的酸性均依次增强 |
| D.元素周期表中位于金属和非金属分界线附近的元素称为过渡元素 |
下列排列顺序正确的是:
①热稳定性:H2O>HF>H2S②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4④非金属性:S>O>F
⑤碱性:NaOH>Mg(OH)2>Al(OH)3
| A.①③ | B.②⑤ | C.①④ | D.②③ |
下列说法正确的是:
| A.SiH4比CH4稳定 | B.Na和Cs属于ⅠA族元素,Cs失电子能力比Na的强 |
| C.O2―半径比F―的小 | D.P和As属于ⅤA族元素,H3PO4酸性比H3AsO4的弱 |
简单原子的原子结构可用下图的表示方法来形象表示,其中 表示质子或电子,
表示质子或电子, 表示中子。则下列有关①②③的叙述中正确的是:
表示中子。则下列有关①②③的叙述中正确的是:
| A.①、②、③互为同位素 | B.①、②、③互为同素异形体 |
| C.①、②、③是三种化学性质不同的粒子 | D.①、②、③具有相同的质量数 |
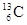 -NMR(核磁共振)可用于含碳化合物的结构分析,
-NMR(核磁共振)可用于含碳化合物的结构分析,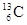 表示的含义是:
表示的含义是:
| A.核内有6个质子,核外有13个电子 |
| B.表示碳元素的一种单质 |
| C.质量数是13,原子序数是6,核内有7个质子 |
| D.质量数是13,原子序数是6,核内有7个中子 |