有机物结构式可以简化,如: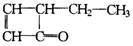 可表示为
可表示为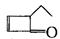 ,某有机物
,某有机物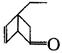 的多种同分异构体中,属于芳香醇的一共有(不考虑立体异构)
的多种同分异构体中,属于芳香醇的一共有(不考虑立体异构)
| A.3种 | B.4种 | C.5种 | D.6种 |
室温下向10mL pH=3的醋酸溶液中加入水稀释后,下列说法正确的是
| A.溶液中导电粒子的数目减少 |
B.溶液中 不变 不变 |
| C.醋酸的电离程度增大,c(H+)亦增大 |
| D.完全中和醋酸需加入10mLpH=11的NaOH溶液 |
下列叙述正确的是
| A.无论是纯水,还是酸性、碱性或中性稀溶液,在常温下,其c(H+)×c(OH-)=1×10-14 |
| B.c(H+)等于1×10-7 mol/L的溶液一定是中性溶液 |
| C.0.2 mol/L CH3COOH溶液中的c(H+)是0.1 mol/L CH3COOH溶液中的c(H+)的2倍 |
| D.强电解质的水溶液中不存在电解质分子 |
根据碘与氢气反应的热化学方程式
(i)I2(g)+ H2(g)  2HI(g)ΔH =-9.48 kJ·mol-1
2HI(g)ΔH =-9.48 kJ·mol-1
(ii) I2(s)+ H2(g) 2HI(g)ΔH = +26.48 kJ·mol-1,下列判断正确的是
2HI(g)ΔH = +26.48 kJ·mol-1,下列判断正确的是
| A.254g I2(g)中通入2gH2(g),反应放热9.48 kJ |
| B.1 mol固态碘与1mol气态碘所含的能量相差17.00 kJ |
| C.反应(i)的产物比反应(ii)的产物稳定 |
| D.反应(ii)的反应物总能量比反应(i)的反应物总能量低 |
已知:CO2(g) + 3H2(g) 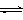 CH3OH(g) + H2O(g) ΔH =-49.0 kJ•mol-1。一定条件下,向体积为1 L的密闭容器中充入1 mol CO2和3 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中,正确的是
CH3OH(g) + H2O(g) ΔH =-49.0 kJ•mol-1。一定条件下,向体积为1 L的密闭容器中充入1 mol CO2和3 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中,正确的是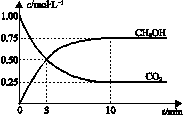
A.升高温度能使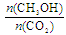 增大 增大 |
| B.反应达到平衡状态时,CO2的平衡转化率为75% |
| C.3 min时,用CO2的浓度表示的正反应速率等于用CH3OH的浓度表示的逆反应速率 |
| D.从反应开始到平衡,H2的平均反应速率υ(H2)=0.075 mol•L-1•min-1 |
用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一物质中(括号内),溶液能与原来溶液完全一样的是
| A.CuSO4 [Cu(OH)2] | B.NaOH [NaOH] | C.NaCl [盐酸] | D.AgNO3 [Ag2O] |