有A、B、C、D四种金属,当A、B组成原电池时,电子流动方向A →B ;当A、D组成原电池时,A为正极;B与E构成原电池时,电极反应式为:E2-+2e-=E,B-2e-=B2+则A、B、D、E金属性由强到弱的顺序为
A.A>B>E>D B.A>B>D>E
C.D>E>A>B D.D>A>B>E
下列四组实验,根据实验事实得出的结论,正确的是
| A.在未知试液中滴加BaCl2溶液得白色沉淀,取该白色沉淀加稀盐酸不溶解,说明原未知试液中含有SO42- 。 |
| B.在五水硫酸铜中滴加少量浓硫酸,固体颜色由蓝变白,说明浓硫酸具有吸水性 |
| C.在铜片上滴加少量稀硫酸,无明显现象,说明稀硫酸没有氧化性 |
| D.某未知气体通入品红溶液中,品红溶液褪色,则原气体一定是 SO2 |
对于下列事实的解释错误的是
| A.常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应 |
| B.浓硝酸在光照下颜色变黄,说明浓硝酸不稳定 |
| C.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 |
| D.向碘水中滴加CCl4,振荡静置分层,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘 |
已知:①硫酸比次氯酸稳定;②高氯酸是比硫酸更强的酸;③S2-易被氯气氧化;④氯化氢比硫化氢稳定;⑤稀盐酸不跟铜反应,浓硫酸能跟铜反应。上述叙述中可说明氯元
素比硫元素非金属性强的是
| A.①②③ | B.②③④ | C.③④⑤ | D.①③⑤ |
在常温常压下,a, b,c,d 四支相同的试管中,分别装入以等物质的量混合的两种气体。a试管内是NO2和O2,b试管内是C12和SO2,c试管内是NO和O2,d试管内是O2和H2。将四支试管迅速同时倒立于水中,最终水面上升高度h的比较,正确的是
| A.hb>hc>ha>hd | B.hc>ha>hb>hd | C.hd>ha>hc>hb | D.hb>ha>hc>hd |
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ·mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) △H=-192.9kJ·mol-1
下列说法正确的是
| A.根据反应①,64gCH3OH完全燃烧放出的热量为98kJ |
B.反应①中的能量变化如图所示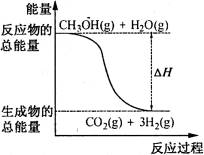 |
| C.CH3OH转变成H2的过程一定要吸收能量 |
| D.根据②推知反应CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g)的△H>-192.9kJ·mol-1 |