纯碱是一种重要的盐类物质,在化学工业中用途极广。小红同学为探究纯碱的化学性质进行了猜想,并设计实验进行验证。请你帮助她将下列实验报告填写完整。
| 猜想 |
实验操作 |
实验现象 |
结论(或化学方程式) |
| 猜想一:纯碱溶液显碱性 |
|
溶液变红 |
纯碱溶液显碱性 |
| 猜想二:能与盐酸反应 |
取少量纯碱溶液于试管中,滴加稀盐酸 |
|
化学方程式: |
| 猜想三:能与石灰水反应 |
取少量纯碱溶液于试管中,滴加澄清石灰水 |
|
化学方程式: |
| 猜想四:能与氯化钡溶液反应 |
取少量纯碱溶液于试管中,滴加氯化钡溶液 |
|
化学方程式: |
【交流与反思】若用稀硫酸代替稀盐酸进行实验,与猜想二相同,原因是 。
过氧化钠(Na2O2)是一种淡黄色固体。在一次科技活动中,某化学兴趣小组的同学将包有Na2O2固体的棉花放入了如图1的实验中,发现了高低不同的两根蜡烛,下面的蜡烛先熄灭,上面的蜡烛后熄灭;同时也惊奇地发现棉花燃烧了起来。
(1)实验过程中“下面的蜡烛先熄灭,上面的蜡烛后熄灭”的现象说明二氧化碳具有
、 的性质。
(2)棉花为什么会燃烧呢?小组同学认为棉花要燃烧,除了满足“棉花是可燃物”这一条件,还另需满足a: 、 b: 两个条件。
[提出问题]:在上述实验中是如何给棉花提供a和b这两个燃烧条件的呢?
[查阅资料]:1、在常温下Na2O2和CO2能发生化学反应。
2、无水硫酸铜为白色固体,吸水后变为蓝色。
[设计实验]:经过讨论后,小组同学设计了如下图2的实验进行探究。

[实验步骤]:①检查整套装置的气密性;②把相关的试剂放入对应的仪器内(D装置的U型管内放有足量的Na2O2固体,烧杯内盛有饱和的澄清石灰水),并按图2组装整套实验仪器;③用力推动针筒的活塞,把稀盐酸注入试管内;④一段时间后,在P处放置一根带火星的小木条,观察现象。
注:整个实验中不考虑稀盐酸的挥发和空气对实验的影响。
[实验现象]:①无水硫酸铜没有变蓝色;②带火星的小木条复燃;③饱和的澄清石灰水变浑浊。
[实验分析]:①浓硫酸的作用是: 。
②D装置的烧杯内澄清石灰水变浑浊的原因是 。
[得出结论]:①“小木条复燃”说明Na2O2和CO2反应产生的一种气体,使图1中的棉花满足了燃烧的一个条件;②“饱和的澄清石灰水变浑浊”说明Na2O2和CO2反应将 能转化为热能,使图1中的棉花满足了燃烧的另一个条件。
[拓展提高]:①Na2O2和CO2反应除生成一种气体外,还生成了一种固体,小明认为生成的固体是NaOH,小红认为是Na2CO3,同学们经过思考后认为 同学的猜想是错误的,理由是: 。
②Na2O2和CO2反应的化学方程式是 。
A、B、C是初中化学常见的液体、气体、固体,气球套在试管口且保证密封性能良好。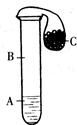
(1)若A能使紫色石蕊变红,B为空气,将固体C倒入试管中产生气泡,同时气球因膨胀而鼓起来。液体A,固体C可能是什么物质?请给出两种不同组合(C为不同类别物质),组合一:_________,化学方程式 ;组合二:_______,化学方程式_________。
根据下列装置图,回答有关问题:
(1)写出图中标号仪器的名称:a ,b 。
(2)若制取氢气,可选用的发生装置是 (填字母)。
(3)点燃不纯的可燃性气体可能发生爆炸。下图是某同学的改进装置:下图是可燃性气体的洗气改进装置,检查它的气密性的方法是:向导管a处 ,若 则气密性好;若在导管a处通入可燃性气体,在导管b处连上尖嘴管并松开止水夹,点燃,即使气体不纯也不会爆炸,可见此装置的作用是 。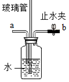
小明买了一种“汽泡爽”的冲调饮料。
【饮料说明】
①主要原料:柠檬酸(C6H8O7)和小苏打(NaHCO3);
②使用说明:将一包“汽泡爽”粉末倒入玻璃杯中,加入200 mL冷水,看到有大量气泡快速生成,待粉末完全溶解,就得到一杯果味饮料。
小明观察了饮料说明后,他借助化学实验的方法,探究“汽泡爽”产生气体的成分,以及加水温度对产生气体量的影响。
【实验一】探究“汽泡爽”产生气体的成分。
(1)小明阅读资料发现:“汽泡爽”原料中的柠檬酸(C6H8O7)和小苏打(NaHCO3)粉末混合后加水,可以发生以下反应,填写生成气体的化学式。
3NaHCO3 + C6H8O7 ="===" C6H5O7Na3 + 3H2O + 3 ↑
(2)为了检验该气体,小明选择的试剂是 。
【实验二】探究加水温度对产生气体量的影响。
(1)小明先用冷水和热水各冲了一杯饮料,品尝时发现冷水冲的饮料中气泡较多,热水冲的饮料中气泡较少。当他摇动杯子时,发现有大量气泡从水中逸出。他查阅资料发现:随着温度升高,气体在一定量的水中溶解的量会迅速降低。于是小明设计了如下实验方案,请填写表中空白。
| 实验序号 |
加入水的体积 |
加入水的温度 |
收集到的气体的体积 |
| 1 |
200 mL |
15℃ |
a(待记录) |
| 2 |
|
50℃ |
b(待记录) |
(2)在老师的帮助下,小明采用相同的两套实验装置(如下图)分别完成上述实验,在A中加入水,再加入一袋“汽泡爽”,迅速塞紧胶塞。量筒C用于收集A中产生的气体所排出的液体,冷却至室温后读取数据。B中油层的作用是 。
(3)通过实验,小明测得:a =" 64" mL,b =" 132" mL,由此获得结论:“汽泡爽”产生气体的量与加水温度有关系。但是老师看到小明的实验报告后却指出:两套装置中,“汽泡爽”产生气体的总量应该近似相等,与温度关系不大,其本质原因是 。
(4)通过反思,为了证明老师的观点,小明继续利用(3)中已反应完的两套装置,又做了一步实验,发现两套装置最终收集到的气体的总量确实相近,他的实验操作是 。
人类每年都要从大自然中提取大量的金属,用于满足日常生活和工农业生产的需要。
⑴某铁厂以焦炭、赤铁矿石(主要含Fe2O3)、空气等为原料炼铁,反应过程如下:
上述工艺流程中,步骤③发生反应的化学方程式为 ,
该反应中的还原剂是 。
⑵实验室常用下图装置模拟炼铁反应,实验开始时,须先通 CO,再用酒精喷灯加热,这样做的目的是 。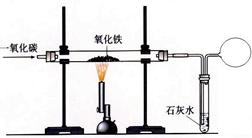
⑶我国古代即有湿法冶金技术,古书中就有“曾青得铁则化为铜”之说,请你写出铁能从硫酸铜溶液中置换出铜单质的原因: 。
⑷在众多的金属材料中,铝及其合金一直在人类生产、生活中占据着主导地位,工业上常采用电解氧化铝的方法来冶炼铝,该反应的化学方程式为 。