某校化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,设计出了如图所示的实验装置。实验步骤如下:(每小格1分,共4分)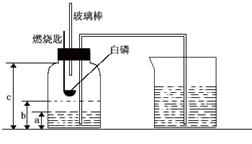
①如图所示,连接仪器,发现装置的气密性良好。
②在集气瓶里装a 体积的水,燃烧匙里放一块白磷并在酒精灯上把玻璃棒下端加热,把长导管的另一端放入盛有足量水的烧杯中。
③用力把预先加热过的玻璃棒按下与白磷接触,观察到白磷立即着火燃烧,产生大量白烟,同时放出大量的热。
⑤待集气瓶完全冷却至室温,量出集气瓶中水的体积是b,整个集气瓶的体积是c。
⑥根据a.b.c三个数据,计算出空气中氧气的体积分数。回答下列问题。
(1)在白磷开始燃烧到最后熄灭的过程中,集气瓶内水面的变化情况是 。
(2)若实验非常成功,请写出a.b.c三个数据应满足的一个等式关系式: 。
(3)组内成员小张对“实验前集气瓶里要装进适量a 体积的水”非常不理解。咨询了组长小明之后,他终于明白“a 体积的水”的作用,其一是为了加快⑤步骤中集气瓶的冷却速度;其二则主要是 。
(4)在上述实验中,下列操作的实施和实验现象的出现,会导致实验最后产生的实际值大于理论值的是
| A.装置气密性不好 |
| B.实验前集气瓶里没有装a体积的水 |
| C.集气瓶没有冷却到室温 |
| D.用红磷代替白磷(红磷的着火点在240℃左右) |
科学家设想利用太阳能加热器"捕捉
"、"释放
",实现碳循环(如图所示)。
某化学小组的同学对此非常感兴趣,在老师的指导下,设计如下装置探究上述设想的反应原理是否可行。
(1)能证明装置
"释放
"的现象是;
(2)装置
在实验结束撤掉酒精喷灯时的作用是;
(3)上述反应结束后,小组同学对
中固体的成分进行探究,以证明是否"捕捉"到
。
【猜想与假设】
中的固体可能为:I.只有氧化钙;Ⅱ.氧化钙与碳酸钙;Ⅲ.只有碳酸钙
【进行实验】
①甲同学从
中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物。甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅲ成立。乙同学认为上述实验不足以证明猜想Ⅲ成立,其理由是。
②乙同学从
中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生。乙同学据此认为试管中的固体只有氧化钙,即猜想I成立。丙同学认为乙的实验不足以证明猜想I成立,理由是。
③丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,他用水、酚酞试液和
稀盐酸证明了猜想Ⅱ成立,请完成他的实验报告。
| 实验步骤 |
实验现象 |
实验结论 |
| 猜想Ⅱ成立 |
(4)通过以上探究,小组同学认为科学家的设想在反应原理上是可行的。该设想的优点有(填字母序号)。
| A. |
原料易得 |
B. |
充分利用太阳能 |
C. |
释放出的 可作为资源加以利用 |
实验是科学探究的重要方法。如图是测定空气中氧气含量实验的两套装置图,请结合图示回答有关问题。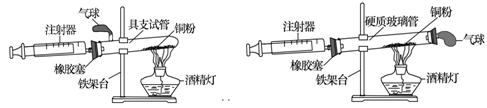
装置一 装置二
(1)根据下表提供的实验数据,完成下表
| 硬质玻璃管中空气的体积 |
反应前注射器中空气体积 |
反应后注射器中气体体积 |
实验测得空气中氧气的体积分数 |
| 25 | 15 | 9 |
(2)装置一和装置二中气球的位置不同,(填"装置一"或"装置二")更合理,理由是。
(3)若实验测得的结果偏小(氧气的体积分数小于21%),可能的原因有哪些?(列举两条);。
某化学小组查阅资料得知:在不同温度下,甲烷(
)可将氧化铁(
)还原为
、
中的一种可两种。他们为探究甲烷与氧化铁反应后产物(黑色粉末)的成分,进行了如下实验:
(1)按图1装置连接好仪器,检查装置的气密性后,往装置中添加药品。
①各黑色粉末中滴加稀硫酸,观察到有气泡产生,则黑色粉末中含有,产生气泡的化学方程式是。
②导管
的作用是。
(2)按图2装置连接好仪器(图中夹持设备已略去)检查装置的气密性,往装置中添加药品,打开止水夹
通入含有少量二氧化碳的的一氧化碳,持续一段时间后再点燃装置
处的酒精喷灯。
①装置
中反应的化学方程式为,装置
中浓硫酸的作用是。
②持续一段时间后再点燃装置
处的酒精喷灯的原因是。
装置的作用是。
③实验中观察到装置
中石灰水变浑浊,则黑色粉末中含有。尾气处理方法为。
实验室有一瓶长期暴露在空气中的氢氧化钠固体样品,观察发现,样品表面有白色粉末。某兴趣小组的同学对该样品的成分及含量进行了探究。
【提出问题】该样品中含有那些物质?
【提出猜想】通过分析,提出如下猜想:
猜想Ⅰ:已完全变质,该样品中只含
;
猜想Ⅱ:部分变质,该样品中含有
和
。
则
变质反应的化学方程式为。
【查阅资料】
①碱性的
溶液可以与中性的
溶液发生复分解反应;
②CO2在饱和碳酸氢钠溶液中几乎不溶解。
【实验探究1】为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验报告。
| 实验操作 |
实验现象 |
实验结论 |
| (1)取少量样品溶于水,加入; |
白色沉淀产生 |
该反应的化学方程式:; |
| (2)将上述反应后的混合物过滤,取滤液加入。 |
。 |
证明猜想Ⅱ正确 |
【提出问题2】如何测量该部分变质样品中碳酸钠的质量分数?
【实验探究2】小红同学设计如下图所示装置(铁架台略去),实验在27℃,101
下进行,步骤如下:
①按图连接好装置;
②用托盘天平准确称取该样品2
,放入
中试管内,向
中集气瓶中倒入饱和碳酸氢钠溶液至瓶颈处;
③向分液漏斗中加入稀硫酸,打开活塞,让稀硫酸滴入试管中至过量,关闭活塞。反应结束后,量筒中收集到饱和碳酸氢钠溶液220
。
请回答下列问题:
(1)在实验步骤①和②之间,还缺少一实验步骤,该实验步骤是;
(2)
中集气瓶盛放的饱和碳酸氢钠溶液不能用水代替,其理由是;
(3)试管中原有的空气对实验结果是否有明显影响?(填"有"或"没有")
(4)变质氢氧化钠样品中碳酸钠的质量分数为。(在27℃,101
时二氧化碳的密度为1.8
)(计算结果精确至1%)
【提出问题3】怎样提纯该样品得到纯净的氢氧化钠固体?
【实验探究3】为得到纯净的氢氧化钠固体,小亮设计了如下图所示的实验流程。
请回答下列问题:
(1)操作①、②、③的名称分别为,为了使样品充分溶解,操作①中还要用到的玻璃仪器是;
(2)该实验中发生反应的化学方程式为;
(3)最终所得氢氧化钠固体质量变质后样品中氢氧化钠的质量(填"小于"、"等于"或"大于")。
【实验反思】
(1)通过本题,你学会了定性检验氢氧化钠的变质、定量测定变质样品中某成分的含量,以及除杂提纯物质。为了得到可靠的实验结果,探究过程中你需要思考的问题有(填数字序号);
①选择试剂种类②确定试剂用量③试剂产地④实验装置与步骤的设计⑤实验安全环保⑥测量中减少误差
(2)实验探究Ⅰ中的检验和实验探究3中的除杂都将碳酸钠进行了转化,但二者目的不同,分别是。
化学实验是科学探究的重要途径。请根据下列实验图示回答相关问题: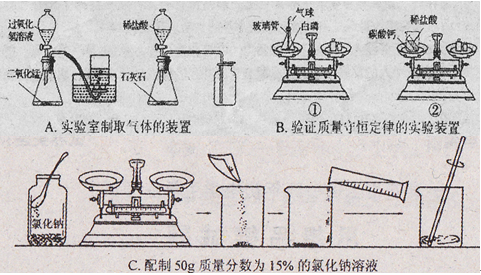
(1)
是实验室制备气体的发生于收集装置。用过氧化氢溶液与二氧化锰制取氧气的化学方程式为,制取氧气、二氧化碳可用同样的发生装置,原因是,选择收集装置的依据是;
(2)
实验中设计合理的是(填"①"或"②"),另一装置设计中存在的问题
是;
(3)
是定量实验,选择仪器不恰当或操作不规范都会导致实验结果有误差。实验时选择量筒规格应
为(填"50mL"或"100mL"),称量时砝码与药品放反了(1g以下为游码),所得溶液的质量分数15%(填"小于"、"等于"或"大于")。