某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是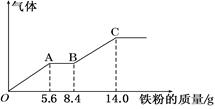
| A.原混合酸中HNO3的物质的量为0.8 mol |
| B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生的是氢气 |
| C.第二份溶液中最终溶质为FeSO4 |
| D.H2SO4的物质的浓度为2.5 mol·L-1 |
氢镍电池是近年开发出来的可充电电池,可以取代会产生隔污染的镉镍电池。氢镍电池的总反应式 H2+NiO(OH)
H2+NiO(OH) Ni(OH)2,根据此反应式判断,下列叙述中正确的是
Ni(OH)2,根据此反应式判断,下列叙述中正确的是
| A.电池放电时,电池负极周围溶液pH不断增大 | B.电池放电时,镍元素被氧化 |
| C.电池充电时,氢元素被氧化 | D.电池放电时,H2是负极 |
能正确表示下列化学反应的离子方程式是
| A.用氢氧化钠溶液吸收少量二氧化硫:2OH-+SO2=SO32-+H2O |
| B.金属铝溶于盐酸中:Al+2H+=Al3++H2↑ |
| C.硫酸铜溶液与氢氧化钡溶液反应:SO42-+Ba2+=BaSO4↓ |
| D.碳酸镁溶于硝酸中:CO32-+2H+=H2O+CO2↑ |
在四个不同的容器中,在不同的条件下进行合成氨反应。根据在相同时间内测定的结果判断,生成氨的速率最快的是
| A.υ(H2)="0.1" mol·L-1·min-1 |
| B.υ(N2)="0.2" mol·L-1·min-1 |
| C.υ(NH3)="0.15" mol·L-1·min-1 |
| D.υ(H2)="0.3" mol·L-1·min-1 |
X、Y、Z、W 4块金属分别用导线两两相连浸入稀硫酸中组成原电池。X、Y相连时,X为负极;Z、W相连时,电流方向是W ® Z;X、Z相连时,Z极上产生大量气泡;W、Y相连时,W极发生氧化反应。据此判断 4种金属的活动顺序是
4种金属的活动顺序是
| A.X>Z>W>Y | B.Z>X>Y>W |
| C.X>Y>Z>W | D.Y>W>Z>X |
反应4NH3(气)+5O2(气)= 4NO(气)+6H2O(气)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率(x)(反应物的消耗速率或产物的生成速率)可表示为
| A.v(NH3)=0.010mol/(L·s) | B.v(O2)=0.0010mol/(L·s) |
C.v (NO)=0.0010mol/(L·s) (NO)=0.0010mol/(L·s) |
D.v(H2O)=0.0045mol/(L·s) |