某强酸性溶液X中含有Ba2+、SiO32-、NH4+、Fe2+、Fe3+、CO32-、SO42-、Al3+、NO3-中的一种或几种离子,取该溶液进行连续实验,能实现如下转化:
根据以上信息,请回答下列问题:
(1)溶液X中除H+外肯定含有的离子是 。不能确定是否含有的离子是 ,若要进一步确定是否含有该离子 。
(2)沉淀E的化学式为 。
(3)实验过程中,属于氧化还原的反应有 个。
(4)写出步骤②中生成溶液F的离子方程式 。
已知镁在空气中燃烧主要生成氧化镁,同时还会与氮气反应生成微量的氮化镁(Mg3N2)在周期表中,镁与锂;铍与铝处于对角线上,处于对角线 上的主族元素性质相似,这称为对角线规则。据此请回答:
上的主族元素性质相似,这称为对角线规则。据此请回答:
(1) 锂在空气中燃烧主要产物的电子式是 _______同时生成微量的____________。(写化学式)
(2)铍的最高价氧化物对应的水化物的化学式是_________________,它属两性化合物,
证明这一结论的有关离子方程式为_______________________,________________________。
(3)若已知反应Be2C+4H2O===2Be(OH)2+CH4↑,则Al4C3遇强碱溶液反应的离子方程式
为________________________________________________。
(4) 用电子式表示BeCl2的形成过程:________________________________________。
(12分)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。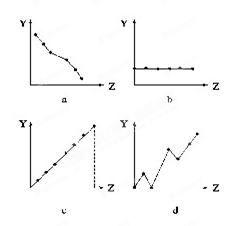
把与下面 元素有关的性质相符的曲线标号填入相应的空格中:
元素有关的性质相符的曲线标号填入相应的空格中:
(1)ⅡA族元素的价电子数____________。
(2)第三周期元素的最高化合价__________。
(3)F-、Na+、Mg2+、Al3+的离子半径________。
(4) 第三周期元素的电负性____________。
(10分)已知某溶液中只存在OH-、H+、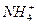 、Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
、Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
①c(Cl一)>c(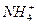 )>c(H+)>c(OH-)②c(Cl一)>c(
)>c(H+)>c(OH-)②c(Cl一)>c(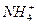 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
③c(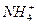 )>c(Cl-)>c(OH-)>c(H+)④c(Cl-)>c(H+)>c(
)>c(Cl-)>c(OH-)>c(H+)④c(Cl-)>c(H+)>c(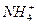 )>c(OH-)
)>c(OH-)
填写下列空白:
(1)若溶液中只溶解了一种溶质,则该溶质是_________________,上述四种离子浓度的大小顺序为______________________(填序号)。
(2)若上述关系中③是正确的,则溶液中的溶质为____________________________________;
若上述关系中④是正确的,则溶液中的溶质为_______________________________________。
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好混合后溶液呈中性,则混合前c(HCl)_______________c(NH3·H2O)(填“大于”“小于”或“等于” )。
)。
氯化铁水解的离子方程式为 _______________,
_______________,
配制氯化铁溶液时滴加少量盐酸的作用是___;
若向氯化铁溶液中加入碳酸钙粉末,发现碳酸钙逐渐逐渐溶解,并产生无色气体,其离子方程式为,
同时有红褐色沉淀生成的原因是、
把FeCl3溶液蒸干后再灼烧,最后得到的主要固体产物是
(8分)A、B代表不同物质,都是H、N、O三种元素组成的强电解质,A、B的水溶液都呈酸性,且相同浓度时,A溶液抑制水的电离,B溶液中促进水的电离。
(1)写出化学式A________, B________;
(2)室下,当A、B两溶液PH均为4时,两溶液中水电离出的氢离子的物质的量浓度之比为1:_;
(3)写出0.1  B溶液中离子浓度由大到小排序;
B溶液中离子浓度由大到小排序;