下列有关糖类、油脂、蛋白质的说法中正确的是()
A、都只由C、H、O三种元素组成 B、都是食物中的基本营养物质
C、都能发生水解反应D、都能发生银镜反应
下列各组有机物中,只需用水就可以鉴别出来的是()
| A.已烷和苯 | B.乙酸和乙醇 | C.硝基苯和乙醇 | D.四氯化碳和溴苯 |
下列有关表达式中不正确的是()
A.乙烷的电子式: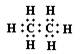 |
B.乙烯的结构式: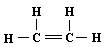 |
C.乙醇的结构式: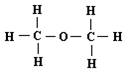 |
D.乙酸的结构简式:CH3COOH |
淀粉和纤维素都可以用(C6H10O5)n表示其分子组成,它们是()
| A.同分异构体 | B.同系物 | C.同种物质 | D.多糖类物质 |
下列物质中能导电的是()
| A.蔗糖溶液 | B.乙醇溶液 | C.乙酸溶液 | D.乙酸乙酯 |