下列说法正确的是
| A.HClO中氯元素化合价比HClO4中氯元素化合价低,所以,HClO4的氧化性强 |
| B.已知①Fe + Cu2+ = Fe2+ + Cu;②2Fe3+ + Cu = 2Fe2+ + Cu2+,则氧化性强弱顺序为: Fe3+ > Cu2+> Fe2+ |
| C.已知还原性:B-> C-> D-,反应 2C-+ D2 = 2D-+C2和反应 2C-+ B2 =2B-+C2都能发生 |
| D.具有强氧化性和强还原性的物质放在一起就能发生氧化还原反应 |
下列物质反应后一定有+3价铁生成的是
①过量的Fe与Cl2反应;
② Fe与过量稀H2SO4反应后,再向其中加KNO3;
③Fe(NO3)2溶液中加少量盐酸;
④Fe和Fe2O3的混合物溶于盐酸中。
| A.只有①② | B.只有②③ | C.只有①②③ | D.全部 |
用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U形管)构成一个原电池。以下有关该原电池的叙述正确的是
①正极反应为:Ag++e-="Ag" ②将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
③实验过程中取出盐桥,原电池仍继续工作 ④在外电路中,电流由铜电极流向银电极
| A.①② | B.②④ | C.②③ | D.③④ |
某物质溶于水,所得溶液既能使蓝色石蕊试液变红,也能与碳酸盐反应生成气体,此物质可能是①氧化物②盐③碱④单质⑤酸中的
| A.①⑤ | B.①②④⑤ | C.② | D.①②③④⑤ |
在标准状况下,将V L 某气体(摩尔质量是M g/mol)溶于0.1 L水中(无化学反应),所得溶液的密度为d g/cm3,则此溶液的物质的量浓度为
A.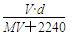 |
B.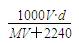 |
C.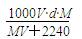 |
D.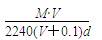 |
用10 mL 0.1 mol/L的BaCl2溶液可分别使相同体积的Fe2(SO4)3、ZnSO4和K2SO4三种溶液中的SO42-完全转化为BaSO4沉淀,则三种硫酸盐溶液的物质的量浓度之比是
| A.1∶3∶3 | B.1∶2∶3 | C.3∶2∶2 | D.3∶1∶1 |