在过量的稀硫酸溶液中加入5.6 g Fe粉,待反应完全后,再加入50 mL0.5mol·L-1 KNO3溶液,恰好反应完全。该反应的方程式为: “ FeSO4 + KNO3 + H2SO4= K2SO4 + Fe2(SO4)3+ NxOy + H2O”,则对该反应的下列说法正确的是
| A.反应中还原产物是NO |
| B.氧化产物和还原产物的物质的量之比为1∶8 |
| C.反应过程中转移的电子数为4e- |
| D.化学方程式中按物质顺序的计量数是:8、2、5、1、4、1、5 |
下列实验操作或装置符合实验要求的是()
| A. |
|
B. |
|
| C. |
|
D. |
|
亚氨基锂(
)是一种储氢容量高、安全性好的固体储氢材料,其储氢原理可表示为:
 ,下列有关说法正确的是
,下列有关说法正确的是
| A. |
中
的化合价是 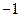 |
B. | 该反应中 既是氧化剂又是还原剂 |
| C. | 和 的离子半径相等 | D. | 此法储氢和钢瓶储氢的原理相同 |
在 1的溶液中,能大量共存的一组离子或分子是
| A. | 、 、 、 | B. | 、 、 、 |
| C. | 、 、 、 | D. | 、 、 、 |
下列液体均处于25 ,有关叙述正确的是()
| A. | 某物质的溶液 <7 |
| B. | =4.5的番茄汁中 是 =6.5的牛奶中 的100倍 |
| C. | 在同浓度的 和 溶液中的溶解度相同 |
| D. | =5.6的 与 混合溶液中, > |
化学已渗透到人类生活的各个方面。下列说法不正确的是
| A. | 阿司匹林具有解热镇痛作用 |
| B. | 可以用 、 制作高温结构陶瓷制品 |
| C. | 在入海口的钢铁闸  门上装一定数量的铜块可防止闸门被腐蚀 门上装一定数量的铜块可防止闸门被腐蚀 |
| D. | 禁止使用四乙基铅作汽油抗爆震剂,可减少  汽车尾气污染 汽车尾气污染 |