碳纳米管是近年来材料科学研究的热点。为除去碳纳米管中的杂质——碳纳米颗粒(少量碳原子的聚集体),可以将样品溶解于强酸性的K2Cr2O7溶液中充分反应,当溶液由橙色转变为绿色(Cr3+)即可,同时放出一种无毒的气体。以下判断正确的是
| A.可以用浓盐酸调节K2Cr2O7溶液的酸性 |
| B.可以通过过滤的方法最终得到碳纳米管 |
| C.该过程中每氧化2 mol碳纳米颗粒,转移8NA个电子 |
| D.若将该反应设计为原电池,则碳纳米颗粒应作为原电池的正极 |
下列叙述中,可用来判断元素金属性强弱的是()
| A.元素最高价氧化物对应水化物的碱性强弱 |
| B.元素最高价氧化物对应水化物的酸性强弱 |
| C.1 mol金属单质与酸反应失去电子的多少 |
| D.1 mol金属单质与水反应放出氢气体积的多少 |
下列试剂中能将NaCl、NH4Cl和FeCl3 三种溶液区分开的是()
| A.HNO3溶液 | B.HNO3溶液 |
| C. NaOH溶液 | D.AgNO3溶液 |
对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法不正确的是()
| A. Zn是负极 | B.Cu是正极 |
| C.负极上发生氧化反应 | D.正极上发生氧化反应 |
在某一化学反应中,反应物A的浓度在10 s内从0.8 mol / L变为0.2 mol / L,则在这10 s内A的化学反应速率为()
| A.0.02 mol / L | B.0.02 mol / (L·s) |
| C.0.06 mol / L | D.0.06 mol / (L·s) |
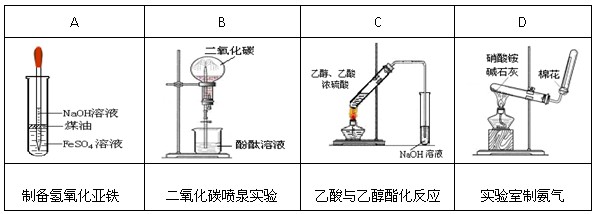
下列药品和装置合理,能完成相应实验的是( )