研究性学习小组用Na2SO3与硫酸溶液(硫酸与水体积比1:1)制备SO2并进行性质探究实验。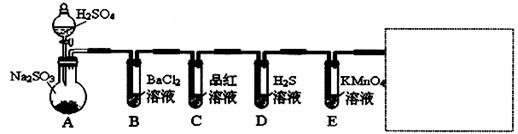
(1)D中的实验现象是:________________,C,E中溶液都褪色,分别体现SO2__________性质。
(2)请在方框中画出收集SO2以及尾气处理装置(标相关试剂)
(3)研究小组发现B中有白色沉淀,为了清楚沉淀的物质,研究小组往B中加入过量稀盐酸,沉淀不溶解,你认为留下的沉淀物是______________,形成该沉淀的总反应的离子方程式为:_____________
为了进一步验证沉淀原因,研究小组另取BaCl2溶液,加热煮沸,冷却及时加入少量苯液封,然后再通SO2,结果发现沉淀量减少,但仍有轻微浑浊。研究小组改进A装置(如图),再进行试验,B中没有出现浑浊。下列气体可以作为X气体的是________(填序号,不定项选择)
| A.CO2 | B.NH3 | C.O3 | D.N2 E.NO2 |
(4)SO2为空气污染物,研究小组为测定某工厂区空气中SO2的含量,取10m3(标准状况),缓慢通过足量溴水中,在所得溶液中加入过量BaCl2溶液,将产生的白色沉淀洗涤,干燥,用电子称称其质量为0.233g,则:
①沉淀洗涤要干净,检验洗涤沉淀已经干净的实验操作是_______________________.
②试计算此空气中SO2的浓度(列出计算表达式并计算结果,结果单位用mg/m3表示)。__________。
(6分)如下图所示的装置,在盛有水的烧杯中,铁圈和银圈的相接处吊着一根绝缘的细丝,使之平衡。小心地从烧杯中央滴入CuSO4溶液。
(1)片刻后可观察到的现象是_________ (指悬吊的金属圈)。
| A.铁圈和银圈左右摇摆不定 |
| B.保持平衡状态不变 |
| C.铁圈向下倾斜 |
| D.银圈向下倾斜 |
(2)产生上述现象的原因是_________。
银及银合金材料是“神七”问天携带研究材料之一。银是日常生活中常见的金属,如银元、银手饰、银器等。
I.某研究性学习小组,设计实验探究某银元中银的质量分数(银元主要成分是银,含少量铜杂质)。取一块银元称质量为Wg,溶于足量的稀硝酸中,充分反应后,在溶液中滴加过量的盐酸,过滤、洗涤、烘干、称重得到固体质量为ag。
(1)根据上述数据,计算该银元中银的质量分数为 。
(2)下列情况使测定银元中银的质量分数偏高 。
A.烘干时,温度偏高B.加入盐酸不足
C.沉淀没有洗涤干净D.加入硝酸溶液浓度过大
II.原子利用率是衡量化学反应绿色化的重要依据之一,原子利用率= 。硝酸银是中学重要化学试剂,某同学利用瓶胆上银制取硝酸银:
。硝酸银是中学重要化学试剂,某同学利用瓶胆上银制取硝酸银:
方案1用14mol/L硝酸溶液溶解银制硝酸银;方案2用2mol/L硝酸溶液溶解银制硝酸银。
(3)写出化学方程式:方案1 。
(4)方案1原子利用率为 ;方案2原子利用率为 。
你认为符合绿色化学要求的方案是 ,理由是 。
(5)已知硝酸银固体受热易分解,硝酸银溶解度变化规律类似硝酸钾的溶解度变化规律。
从硝酸银溶液中分离硝酸银的方法是 。
①冷却热饱和硝酸银溶液,结晶;②蒸发溶剂,结晶。
除去硝酸银晶体表面杂质,适宜采用下列方法: 。
A.用蒸馏水洗涤B.用75%酒精洗涤
C.用饱和硝酸钠溶液洗涤D.用四氯化碳洗涤
除去硝酸银晶体表面的水份,下列措施合适的是 。
a.加热烘干b.吹气凉干c.用滤纸吸干
2008年10月14日长江商报报道:湖北监利钒污染致近千人患严重皮肤病。监利县有投产和在建的非法钒冶炼厂达9家,非法钒冶炼厂所造成的污染使得草木枯萎,饮水变咸,清河变浊,人畜奇怪病变,曾经的鱼米之乡正受到前所未有的污染威胁。钒和钒(V)的化合物在工业上有重要用途。如五氧化二钒是工业接触法制硫酸的催化剂。查阅资料知,利用钒矿石制五氧化二钒和钒的工艺流程图如下:
(1)钒(V)的原子序数为23,下列对钒在元素周期表中位置和元素类别判断正确的是。
A.它位于第五周期第ⅤB族 B.它位于第四周期第ⅤB族 C.它是过渡元素
D.它位于第五周期第ⅤA族 E.它位于第四周期第ⅤA族 F.它与铁位于同一周期
(2)工业上,接触法制硫酸在接触室里发生反应:2SO2+O2 2SO3,催化剂一般是V2O5,下列对五氧化二钒作用的描述正确的是。
2SO3,催化剂一般是V2O5,下列对五氧化二钒作用的描述正确的是。
A.能增大该反应所需要的能量 B.能提高二氧化硫的转化率
C.能改变该反应的反应热(△H) D.能同程度增大正、逆反应速率
E.能增加SO2和O2分子的能量
(3)写出下列化学方程式:
反应I:;反应III:;反应IV:。
(4)预测反应II发生的原因是;IV的反应类型是。
已知:①通常Br2与“C=C”双键起加成反应,但高温下Br2易取代与“C=C”双键直接相连的α-碳原子上的氢原子:
②与苯环直接相连的支链碳原子上的氢原子也易被溴取代: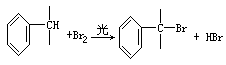
③卤代烃在一定条件下可以水解成醇:
卤代烃也可在一定条件下发生消去反应生成烯烃:
</PGN0069B.TXT/PGN>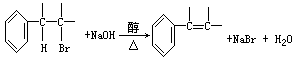
根据上述有关知识推断如何从正丙苯制取1-苯基丙三醇:C6H5—CHOH—CHOH—CH2OH,写出各步反应方程式(注明反应条件)。
磷化氢(PH3)是无色剧毒气体(沸点-89.7℃,其中含微量P2H4而易自燃。其制取原理类似于实验室制氨气,现用下图装置制取PH3并验证其性质。请回答:
(1)用碘化磷(PH4I)和烧碱反应制取PH3的化学方程式______。
(2)实验开始时,先从分液漏斗中往盛有碘化磷的烧瓶A中加入过量乙醚(无色液体,沸点34.5℃,微溶于水,不与Fe2(SO4)3反应),微热数分钟后再从分液漏斗中向烧瓶里加入一定量的浓NaOH溶液继续加热。在B处用电热器控制温度在300℃左右,实验过程中可观察到:
①用水冷却的C中有白色蜡状固体生成。
②D试管中Fe2(SO4)3溶液的颜色由棕黄色变成淡绿色,同时也有白色蜡状物生成。
③E处点燃尾气,呈淡蓝色火焰。则:
C中的白色蜡状固体是(填分子式)______,能说明PH3具有______性质。试管D中反应的化学方程式是______,说明PH3具有______性。
(3)实验时E处尾气须点燃,原因是______。
(4)实验开始时,先向烧瓶中加入乙醚并微热,其目的是______。
(5)D中液面上有少量乙醚层,出现的原因是______