甲、乙两容器都发生反应2 A(g)+B(g) 3C(g),两容器温度和初始压强都相同。在甲恒容容器中充入2 mol A和1 mol B,达平衡后,C在平衡混合气中的体积分数为φ1、物质的量为n1;在乙恒压容器中充入1.4 mol A、0.7 mol B和0.6 mol C,达平衡后C在平衡混合气中的体积分数为φ2、物质的量为n2。下列说法中正确的是
3C(g),两容器温度和初始压强都相同。在甲恒容容器中充入2 mol A和1 mol B,达平衡后,C在平衡混合气中的体积分数为φ1、物质的量为n1;在乙恒压容器中充入1.4 mol A、0.7 mol B和0.6 mol C,达平衡后C在平衡混合气中的体积分数为φ2、物质的量为n2。下列说法中正确的是
A.φ1>φ2 B.n1>n2 C.n1=n2 D.φ1<φ2
下列叙述正确的是
A.危险化学品标志中的数字表示该危险品的危害程度,数字越大危害越大 |
B.二氧化硅晶体被广泛用于制作太阳能电池和光导纤维 |
C.根据分散质在分散剂中均匀分布时间的长短把分散系进一步分为溶液、胶体和浊液 |
D.钢材和硬币都是合金,若改变这些合金的原料配比会改变这些合金的性能 |
有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成原电池。电池的总反应类似于CH4在O2中燃烧,则下列说法正确的是()
①每消耗1molCH4可以向外电路提供8mole-
②负极上CH4失去电子,电极反应式CH4+10OH--8e-=CO32-+7H2O
③负极上是O2获得电子,电极反应式为O2+2H2O+4e-=4OH-
④电池放电后,溶液PH不断升高
| A.①② | B.①③ | C.①④ | D.③④ |
已知四种强电解质溶液,分别含有下列阴、阳离子中的各一种,并且互不重复:NH 、Ba2+、Na+、H+、SO
、Ba2+、Na+、H+、SO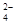 、NO
、NO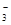 、OH-、CO
、OH-、CO 。将这四种溶液分别标记为A、B、C、D,进行如下实验:
。将这四种溶液分别标记为A、B、C、D,进行如下实验:
①在A或D中滴入C,均有沉淀生成
②D和B反应生成的气体能被A吸收
③A和D反应生成的气体能被B吸收
试回答下列问题:
(1)D的化学式是
(2)写出B物质的化学式:
(3)写出实验②中有关反应的离子方程式
。
由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、C1—、NH4+、Mg2+、CO32-、Ba2+、SO42—。将该混合物溶于水后得澄清溶液,现取3份100mL该溶液分别进行如下实验:
| 实验序号 |
实验内容 |
实验结果 |
| 1 |
加AgNO3溶液 |
有白色沉淀生成 |
| 2 |
加足量NaOH溶液并加热 |
收集到气体1.12L(已折算成标准状况下的体积) |
| 3 |
加足量BaC12溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 |
第一次称量读数为6.27g,第二次称量读数为2.33g |
试回答下列问题:
(1)根据实验1对C1—是否存在的判断是 (填“一定存在”、“一定不存在”或“不能确定”);根据实验1—3判断混合物中一定不存在的离子是 。
(2)试确定溶液中一定存在的阴离子及其物质的量浓度(可不填满):
| 阴离子符号 |
物质的量浓度(mol·L—1) |
(3)试确定K+是否存在? ,判断的理由是
。
根据下表提供的材料,下列叙述中,正确的是()
| 序号 |
氧化剂 |
还原剂 |
其他反应物 |
氧化产物 |
还原产物 |
| ① |
Cl2 |
FeBr2 |
FeCl2 |
||
| ② |
KMnO4 |
H2O2 |
H2SO4 |
O2 |
MnSO4 |
| ③ |
KClO3 |
HCl(浓) |
Cl2 |
Cl2 |
|
| ④ |
KMnO4 |
HCl(浓) |
Cl2 |
MnCl2 |
| A.表中第①组反应的氧化产物只有FeCl3(实为Fe3+) |
| B.氧化性比较:KMnO4>Cl2>Fe3+>Br2>Fe2+ |
| C.表中第③组反应的氧化产物与还原产物的质量之比为6:1 |
| D.④的离子方程式配平后,H+的化学计量数应为16 |