氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为
a HClO3 = bO2↑+ c Cl2↑+ d HClO4 + e H2O。下列有关说法不正确的是
| A.由反应可确定:氧化性HClO3>O2 |
| B.若氯酸分解所得混合气体,lmol混合气体质量为45g,则反应方程式可表示为:3HClO3 = 2O2↑+ C12↑+ HClO4 + H2O |
| C.由非金属性Cl>S,可推知酸性HClO3>H2SO4 |
| D.若化学计量数a=8,b=3,则该反应转移电子数为20e- |
【原创】下列说法正确的是
| A.氨基酸因为既含有-NH2又含有-COOH,所以氨基酸显两性 |
| B.糖类、油脂、蛋白质都能发生水解,它们是天然高分子化合物 |
| C.乙烯使溴水褪色是因为发生氧化还原反应 |
| D.苯既发生取代反应又能发生加成反应,说明苯分子中含有碳碳双键 |
下列说法正确的是
| A.NaCl常用于调味剂和防腐剂 |
| B.“西气东输”中的“气”指的是煤气 |
| C.食用纯碱可治疗胃酸过多 |
| D.无水乙醇常用作医用消毒剂 |
在体积固定的密闭容器中进行可逆反应2NO2 2NO+O2,下列能作为反应达到平衡状态标志的是
2NO+O2,下列能作为反应达到平衡状态标志的是
①单位时间内生成nmol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2表示的反应速率之比为2∶2∶1
④混合气体的颜色不再改变
⑤混合气体的密度不再改变
⑥混合气体的压强不再改变
⑦混合气体的平均相对分子质量不再改变
| A.①④⑥⑦ | B.②③⑤⑦ | C.①③④⑤ | D.全部 |
双隔膜电解池的结构示意简图如图所示,对该装置及其原理判断错误的是
| A.c隔膜为阴离子交换膜、d隔膜为阳离子交换膜 |
| B.A溶液为硫酸,B溶液为氢氧化钠 |
| C.a气体为氢气,b气体为氧气 |
D.该电解反应的总方程式为:2Na2SO4+6H2O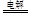 2H2SO4+4NaOH+O2↑+2H2↑ 2H2SO4+4NaOH+O2↑+2H2↑ |
叠氮酸(HN3)与醋酸酸性相似,下列叙述中错误的是
| A.HN3水溶液中微粒浓度大小顺序为:c(HN3)>c(H+)>c(N3-)>c(OH-) |
| B.HN3与NH3作用生成的叠氮酸铵中全都是共价键 |
| C.NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(N3-) >c(OH-)>c(H+) |
| D.N3-与CO2含相等电子数 |