下列关于杂化轨道的叙述中,不正确的是
| A.分子中中心原子通过sp2杂化轨道成键时,该分子不一定为平面三角形结构 |
| B.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子 |
| C.N2分子中N原子没有杂化,分子中有1个σ键、2个π键 |
| D.H2SO4分子中三种原子均以杂化轨道成键 |
根据图所示装置,下列说法不正确的是( )
| 选项 |
开关状态 |
溶液A |
电极B |
说明 |
| A |
打开K1,闭合K2 |
NaCl |
石墨 |
正极反应:O2+2H2O+4e-=4OH- |
| B |
打开K1,闭合K2 |
NaCl |
Zn |
铁制品保护:牺牲阳极的阴极保护法 |
| C |
打开K2,闭合K1 |
CuSO4 |
Cu |
铁表面镀铜 |
| D |
打开K2,闭合K1 |
CuSO4 |
粗铜 |
电解法精炼铜 |
钢铁防腐方法有许多种,如图是其中的一种方法,描述正确的是( )
| A.图中所示是牺牲阳极的阴极保护法 |
| B.铁闸门作阴极,发生还原反应 |
| C.电子流向:a→铁闸门→辅助电极→b |
| D.辅助电极上的反应:O2+2H2O+4e-=4OH- |
某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案: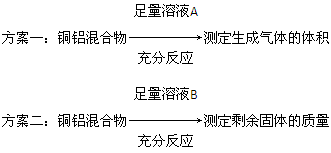
下列有关判断中不正确的是( )。
| A.溶液A和溶液B均可以是盐酸或NaOH溶液 |
| B.若溶液B选用浓硝酸,测得铜的质量分数偏大 |
| C.方案一可能产生氢气,方案二可能剩余铜 |
| D.实验室中方案Ⅱ更便于实施 |
用下列实验装置进行相应实验,能达到实验目的的是( )。
| A.用图1所示装置除去Cl2中含有的少量HCl |
| B.用图2所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
| C.用图3所示装置制取少量纯净的CO2气体 |
| D.用图4所示装置分离CCl4萃取碘水后已分层的有机层和水层 |
用如图所示装置制取表格中的四种干燥、纯净的气体(必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。其中正确的是 ( )。
| 选项 |
气体 |
a |
b |
c |
d |
| A |
SO2 |
浓硫酸 |
Cu |
H2O |
浓硫酸 |
| B |
Cl2 |
浓盐酸 |
MnO2 |
NaOH溶液 |
浓硫酸 |
| C |
NH3 |
饱和 NH4Cl溶液 |
消石灰 |
空集气瓶 |
固体NaOH |
| D |
NO |
稀硝酸 |
铜屑 |
H2O |
浓硫酸 |