某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L H2SO4溶液进行中和热的测定。
Ⅰ.配制0.50 mol/L NaOH溶液
若实验中大约要使用245 mL NaOH溶液,则至少需要称量NaOH固体________g。
Ⅱ.测定中和热的实验装置如图所示
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值57.3 kJ/mol):________ 。
(2)取50 mL NaOH溶液和30 mL硫酸进行实验,实验数据如下表。
①请填写下表中的空白: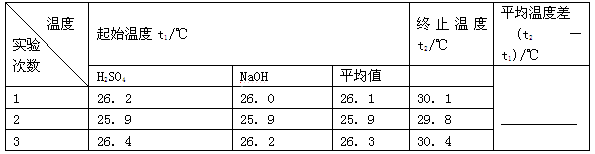
②近似认为0.50 mol/L NaOH溶液和0.50 mol/L H2SO4溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热ΔH=________(取小数点后一位)。
③上述实验结果的数值与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)________。
a.实验装置保温、隔热效果差
b.在量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有稀硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
化学上常用燃烧法确定有机物的组成。下图装置是用燃烧法确定有机物化学式常用的装置,这种方法是在电炉加热时用纯氧氧化管内样品。根据产物的质量确定有机物的组成。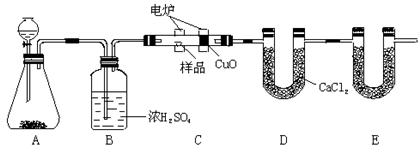
回答下列问题:
(1)A装置中分液漏斗盛放的物质是,写出有关反应的化学方程式:。
(2)C装置(燃烧管)中CuO的作用是。
(3)写出E装置中所盛放物质的名称,它的作用是。
(4)若准确称取1.20g样品(只含C、H、O三种元素中的两种或三种)。经充分燃烧后,E管质量增加1.76g,D管质量增加0.72g,则该有机物的最简式为。
(21分) “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题: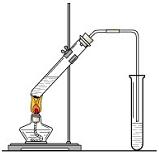
(1)写出制取乙酸乙酯的化学反应方程式
(2)饱和碳酸钠溶液的主要作用是、、。
(3)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是 。
(4)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 。
(5)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是 。
硫酸铜是一种应用极其广泛的化工原料。制备硫酸铜是无机化学实验教学中一个重要的实验。由于铜不能与稀硫酸直接反应,实验中将浓硝酸分次加入到铜粉与稀硫酸中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图1、2所示)。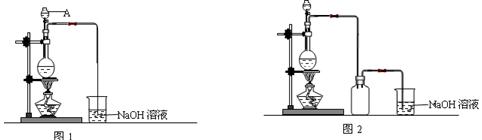
(1)图1中,A仪器的名称为,烧瓶中发生的离子反应方程式为。
(2)图2是图1的改进装置,改进的目的是。
(3)为符合绿色化学的要求,某研究性学习小组进行如下设计:
第一组:空气为氧化剂法
方案1:以空气为氧化剂。将铜粉在仪器B中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应。
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加FeSO4或Fe2(SO4)3,反应完全后,向其中加物质甲调节pH到3~4,产生Fe(OH)3沉淀,过滤、蒸发、结晶,滤渣作催化剂循环使用。(已知Fe(OH)3和Cu(OH)2完全沉淀时的pH分别为3.7、6.4。)
请回答下列问题:
①方案1中的B仪器名称是。
②方案2中甲物质是(填字母序号)。a、CaOb、CuCO3 c、CaCO3
第二组:过氧化氢为氧化剂法
将3.2g铜丝放到45 mL 1.5mol/L的稀硫酸中,控温在50℃。加入18mL 10%的H2O2,反应0.5h后,升温到60℃,持续反应1 h后,过滤、蒸发结晶、减压抽滤等,用少量95%的酒精淋洗后晾干,得CuSO4·5H2O 10.6g。请回答下列问题:
③该反应的离子反应方程式为。
④控制温度在50℃和60℃加热的原因为,晶体采用酒精淋洗的优点是。
⑤上述两种氧化法中,更符合绿色化学理念的是(填“第一组”或“第二组”),理由是。
文献资料显示,草木灰主要含有不溶性杂质及K2CO3,还含有少量KCl、K2SO4等。某化学兴趣小组拟测定草木灰中钾盐的含量及钾盐中K2CO3的含量。
测定草木灰中钾盐含量
(1)该实验的主要步骤顺序为:称量→→→→ →冷却→再称量(填字母序号)
A. 溶解 B.过滤 C、洗涤、烘干 D、蒸发
(2)称量前,在调整托盘天平的零点时,若指针偏向右边,应将右边的螺丝向(填左、右)旋动。某学生称量时,在天平右盘加上规定质量的砝码后,在左盘的小烧杯中加入样品,此时指针稍偏右边,该学生的操作应为。
(3)实验中A、B、C、D三步操作均使用了玻璃棒,操作B中玻璃棒的作用是,操作D用玻璃棒不断搅动的原因。
测定钾盐中K2CO3含量
(4)取上述操作中所得的钾盐,配成稀溶液,加入CaCl2溶液使CO32-生成沉淀,过滤得到碳酸钙沉淀后,用蒸馏水多次洗涤,烘干、称量、计算。检验沉淀是否完全的方法是,检验沉淀是否洗净的方法是。
某校化学小组学生利用“废铁屑与水反应”的产物还原氧化铜,并制取FeCl3·6H2O晶体。(图中夹持、加热及尾气处理装置均已略去)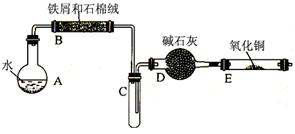
①将5%Na2CO3溶液加入到盛有一定量废铁屑的烧杯中,加热数分钟,用倾析法除去Na2CO3溶液,然后将废铁屑用蒸馏水洗涤2~3遍,用滤纸吸干水分。
②将洗涤干燥后的废铁屑和石棉绒混合置于气密性良好的上述装置B中。
③先点燃X处的酒精灯,待试管C中出现大量水雾时,点燃Y处的酒精喷灯。
④经过必要的实验操作后,点燃Z处的酒精灯。
⑤停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。
⑥利用上述滤液制取FeCl3·6H2O晶体,设计流程如下: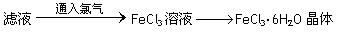
回答下列问题:
(1)实验步骤①的目的是。
(2)步骤③X处是指(用图中的A、B、C……表示),待试管C中出现大量水雾时,点燃Y处的酒精喷灯的目的是:。
(3)步骤④必要的实验操作是指:。
(4)步骤⑥从FeCl3溶液中得到FeCl3·6H2O晶体的主要操作包括:
。
(5)这个流程中需保持盐酸过量,主要原因是:
。