下列有关说法正确的是
| A.反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H<0 |
| B.所有的化学反应都需要一定的活化能来推动 |
C.CH3COOH 溶液加水稀释后,溶液中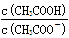 的值增大 的值增大 |
| D.Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH 减小 |
设NA为阿伏加德罗常数的值,下列叙述中正确的是
| A.标准状况下11.2 L NO和11.2 L O2混合后所得气体分子数为NA |
| B.7.1 g Cl2与足量的NaOH溶液反应转移的电子数为0.2NA |
| C.25℃、1.01×105 Pa时,80 g SO3中含有的原子数为4NA |
| D.NA个CO分子和0.5 mol CH4的质量比为7∶4 |
下列实验现象与氧化还原反应有关的是
| A.SO2通入品红溶液中,溶液褪色 |
| B.新制氯水密闭放置一段时间后浅黄绿色消失 |
| C.向Fe2(SO4)3溶液中滴加NaOH溶液,生成红褐色沉淀 |
| D.向硅酸钠溶液中滴加适量的稀盐酸,有透明的凝胶形成 |
下列说法正确的是
| A.胶体区别于其他分散系的本质特征是有丁达尔效应 |
| B.SO3溶于水后所得溶液能导电,所以SO3是电解质 |
| C.SiO2既能与NaOH溶液反应、又能与HF溶液反应,所以SiO2是两性氧化物 |
| D.玻璃和水泥属于硅酸盐材料,都用到石灰石作原料 |
下列物质分类正确的是
| A.H2SO4、NaOH、NaNO3都是电解质 |
| B.Na2O、Al2O3、Fe2O3都是碱性氧化物 |
| C.铝土矿、水玻璃、小苏打都是混合物 |
| D.烧碱、纯碱、熟石灰都是碱 |
下列环境问题与所对应物质无关的是
| A.酸雨——SO2 |
| B.光化学烟雾——NO2 |
| C.水体富营养化——含磷洗涤剂 |
| D.臭氧层破坏——N2 |