室温下,在0.2 mol·L-1 Al2(SO4)3,溶液中,逐滴加入1.0 mol·L-1 NaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图,下列有关说法正确的是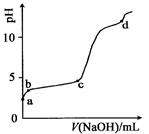
A.a点时,溶液呈酸性的原因是Al3+水解,离子方程式为:Al3++3OH- Al(OH)3 Al(OH)3 |
| B.a~b段,溶液pH增大,Al3+浓度不变 |
| C.b~c段,加入的OH-主要用于生成Al(OH)3沉淀 |
| D.d点时,Al(OH)3沉淀开始溶解 |
铁离子,亚铁离子
工业产品碳酸钠中,常混有氯化钠,测定碳酸钠质量分数的仪器装置如图10-3: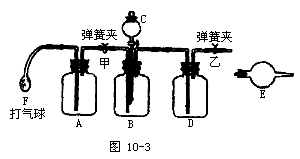
供选用的试剂有:NaOH溶液、饱和石灰水、蒸馏水、浓硫酸、稀硫酸、浓盐酸、稀盐酸、硝酸、碱石灰、无水氯化钙、无水硫酸铜、试样(含有少量氯化钠的碳酸钠)。
请回答:
(1)各有关仪器中使用的药品及作用。
A.____,作用____;B.____,作用____;C.____,作用____;
D.____,作用____;E.____,作用____;F的作用____。</PGN0044B.TXT/PGN>
(2)实验步骤(到得到实验数据止):
①称量:称试样质量及装有干燥剂的球形干燥管的质量,并记录数据。
②____;③____;④____;⑤____;⑥____;⑦____。
为了除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入一种试剂,过滤后再加入适量盐酸。这种试剂是
| A.NH3·H2O |
| B.NaOH |
| C.Na2CO3 |
| D.MgCO3 |
X和Y属短周期元素,X原子的最外层电子数是次外层电子数的一半,Y位于X的前一周期,且最外层只有一个电子,则X和Y形成的化合物的化学式可表示为
| A.XY |
| B.XY2 |
| C.XY3 |
| D.X2Y3 |