部分弱酸的电离平衡常数如下表:
| 弱酸 |
HCOOH |
HCN |
H2CO3 |
| 电离平衡常数(25℃) |
K=1.77×10-4 |
K=4.9×10-10 |
K1=4.3×10-7 K2=5.6×10-11 |
下列说法正确的是
A.0.1mol·L-1 NaHCO3溶液中浓度的大小:c(Na+)>c(HCO3-)>c(H+)>c(OH-)
B.少量的CO2通入到NaCN溶液中:CN-+H2O+CO2 = HCN+HCO3-
C.用0.1mol·L-1 NaOH溶液中和等浓度的HCN和HCOOH时前者所需NaOH溶液体积大
D.相同体积的0.1mol·L-1 HCOONa溶液比0.1mol·L-1 NaCN溶液所含离子总数小
2005年10月12日9时,我国成功发射“神舟六号”载人飞船,遨游太空5天后准确降落。神舟推进舱段安装有4台额定真空推力2500N的轨道控制发动机,推进剂为四氧化二氮和一甲基肼(CH6N2),其主要反应为: CH6N2+N2O4→X+CO2↑+H2O(未配平)。由此可知X中一定含有的元素是
| A.碳 | B.氢 | C.氧 | D.氮 |
2004年4月22日是第35个“世界地球日”,我国确定的主题是“善待地球——科学发展”。下列行为中不符合这一主题的是
| A.采用“绿色化学”工艺,使原料尽可能转化为所需要的物质 |
| B.大量开采地下水,以满足社会对水的需求 |
| C.减少直至不使用对大气臭氧层起破坏作用的氟氯烃 |
| D.节约能源,提高能源利用率 |
两次获得诺贝尔奖,在化学界享有盛名的科学家是()
| A.爱因斯坦 | B.达尔文 | C.居里夫人 | D.欧拉 |
下列广告语在科学性上没有错误的是
| A.这种矿泉水绝对纯净,不含任何离子 |
| B.这种饮料中不含任何化学物质 |
| C.这种口服液含有丰富的氮、磷、锌等微量元素 |
| D.没有水就没有生命 |
观察下图,若用1 L水来代表地球上的总水量,要比较精确地量取地球上的淡水量,应选择的仪器是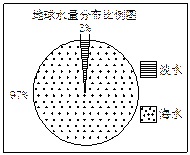
| A.100 mL烧杯 | B.50 mL烧杯 | C.100 mL量筒 | D.50 mL量筒 |