控制适合的条件,将反应Fe3++Ag Fe2++Ag+设计成如图所示的原电池(盐桥装有琼脂—硝酸钾溶液;灵敏电流计的0刻度居中,左右均有刻度)。已知接通后观察到电流计指针向右偏转。下列判断正确的是
Fe2++Ag+设计成如图所示的原电池(盐桥装有琼脂—硝酸钾溶液;灵敏电流计的0刻度居中,左右均有刻度)。已知接通后观察到电流计指针向右偏转。下列判断正确的是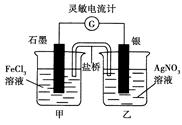
| A.盐桥中的K+移向乙烧杯 |
| B.一段时间后,电流计指针反向偏转,越过0刻度,向左边偏转 |
| C.在外电路中,电子从石墨电极流向银电极 |
| D.电流计指针居中后,往甲烧杯中加入一定量的铁粉,电流计指针将向左偏转 |
将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应H2(g)+Br2(g) 2 HBr(g) ΔH<0平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是()
2 HBr(g) ΔH<0平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是()
| A.a>b | B.a=b | C.a<b | D.无法确定 |
可逆反应:2NO2 2NO+O2在固定体积的密闭容器中反应,不能说明已达到化学平衡状态的是()
2NO+O2在固定体积的密闭容器中反应,不能说明已达到化学平衡状态的是()
| A.单位时间内生成n mol O2的同时生成2n mol NO2 |
| B.混合气体的密度不再改变的状态 |
| C.混合气体的颜色不再改变的状态 |
| D.混合气体的平均相对分子质量不再改变的状态 |
如图所示为某原电池的结构示意图,下列说法不正确的是(盐桥中装满用饱和KCl溶液和琼胶做成的冻胶) ( )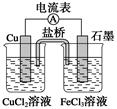
| A.该原电池的总反应式为2Fe3++Cu=2Fe2++Cu2+ |
| B.该电池工作时,Cu2+在电极上得到电子,发生还原反应 |
| C.该电池工作时,氯化铜溶液中氯离子浓度增大 |
| D.电池工作过程中,电子由铜电极经过电流表流向石墨电极 |
一定条件下,合成氨反应达到平衡状态时,按如下操作,平衡不发生移动的是( )
| A.恒T、P时,充入少量的NH3 | B.恒T、V时,充入少量的N2 |
| C.恒T、P时,充入少量的He | D.恒T、V时,充入少量的He |
如下图,各烧杯中盛有海水,铁在其中被腐蚀的速度由快到慢的顺序为 ( )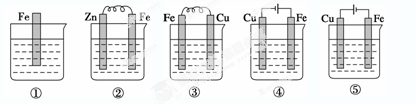
| A.①②③④⑤ | B.④③②①⑤ | C.④③①②⑤ | D.④②③①⑤ |