通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正确的是
| |
现象 |
解释 |
| A |
KI淀粉溶液中通入Cl2,溶液变蓝 |
Cl2能与淀粉发生显色反应 |
| B |
浓HNO3在光照条件下变黄 |
浓HNO3不稳定,生成有色产物NO2能溶于浓硝酸 |
| C |
某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 |
说明该溶液中含有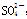 |
| D |
铜片放入浓硫酸中,无明显变化 |
说明铜在冷的浓硫酸中发生钝化 |
“ZEBRA”蓄电池的结构如图所示,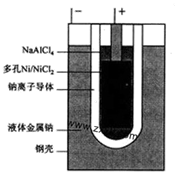
电极材料多孔Ni/NiCl2和金属钠之间由钠离子导体制作的陶瓷管相隔。下列关于该电池的叙述错误的是
| A.电池反应中有NaCl生成 |
| B.电池的总反应是金属钠还原三个铝离子 |
| C.正极反应为:NiCl2+2e-=Ni+2Cl- |
| D.钠离子通过钠离子导体在两电极间移动 |
美国海军海底战事中心与麻省理工大学共同研制成功了用于潜航器的镁过氧化氢燃料电池系统。其工作原理如图所示。以下说法中错误的是 
| A.电池的负极反应为Mg-2e-===Mg2+ |
| B.电池工作时,H+向负极移动 |
| C.电池工作一段时间后,溶液的pH增大 |
| D.电池总反应式是Mg+H2O2+2H+===Mg2++2H2O |
关于原电池、电解池的电极名称,下列说法错误的是
| A.原电池中失去电子的一极为负极 |
| B.电解池中与直流电源负极相连的一极为阴极 |
| C.原电池中相对活泼的一极为正极 |
| D.电解池中发生氧化反应的一极为阳极 |
下列有关溶度积常数Ksp的说法正确的是
| A.常温下,向BaCO3饱和溶液中加入Na2CO3固体,BaCO3的Ksp减小 |
| B.溶度积常数Ksp只受温度影响,温度升高Ksp减小 |
| C.溶度积常数Ksp只受温度影响,温度升高Ksp增大 |
| D.常温下,向Mg(OH)2饱和溶液中加入NaOH固体,Mg(OH)2的Ksp不变 |
下列溶液中各微粒的浓度关系正确的是
| A.pH相等的①NH4Cl②(NH4)2SO4③NH4HSO4溶液,NH4+大小顺序为①>②>③ |
| B.pH相等的NaF与CH3COOK溶液:[c(Na+)-c(F-)]>[c(K+)-c(CH3COO-)] |
| C.0.2 mol·L-1的Na2CO3溶液: c(OH-)=c(HCO3—)+c(H+)+c(H2CO3) |
| D.0.2 mol·L-1 HCl与0.1 mol·L-1 NaAlO2溶液等体积混合:c(Cl-)>c(Na+)>c(Al3+)>c(H+)>c(OH-) |