现有X、Y、Z、W、Q五种短周期元素,其原子序数依次增大,Y、Z、W、Q形成的简单离子具有相同的电子层结构,YX3、X2Z、X2Z2、W2Z、W2Z2都是常见的化合物,其中,YX3在常温下呈气态,能使酚酞溶液变红色。下列有关推断正确的是
| A.简单离子半径:Y>Z>W>Q>X |
| B.W2Z2与X2Z反应中氧化剂与还原剂物质的量之比为1∶2 |
| C.X能分别与Y、Z、Q形成共价化合物 |
| D.Y、W、Q的最高价氧化物对应的水化物两两之间一定相互反应 |
11P + 15CuSO4 + 24H2O = 5Cu3P + 6H3PO4 + 15H2SO4反应中,被氧化的P原子与被还原的P原子个数比是
| A.6:5 | B.5:6 | C.11:5 | D.11:6 |
已知镁和稀硝酸反应时,每有1mol HNO3反应,就有0.8 mol电子转移,此时硝酸的还原产物可能是
| A.N2O | B.NO2 | C.N2O4 | D.NO |
赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿混合加热发生以下反应:Cu2S+2Cu2O=6Cu+SO2↑,关于该反应的说法中,正确的是
| A.该反应的氧化剂只有Cu2O |
| B.Cu2S在反应中既是氧化剂,又是还原剂 |
| C.Cu既是氧化产物又是还原产物 |
| D.每生成19.2g Cu,反应中转移0.6 mol电子 |
硫酸铵在强热条件下分解,生成氨、二氧化硫、氮气和水。反应中生成的氧化产物和还原产物的物质的量之比是
| A.1∶3 | B.2∶3 | C.1∶1 | D.4∶3 |
用0.1 mol / L的Na2SO3溶液30 mL,恰好将2×10-3 mol的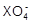 还原,则元素X在还原产物中的化合价是
还原,则元素X在还原产物中的化合价是
| A.+1 | B.+2 | C.+3 | D.+4 |