下列化学表达方式不正确的是
| A.中子数为20的氯原子:37Cl |
B.Cl-的结构示意图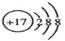 |
C.氢氧根离子的电子式: |
| D.HClO的结构式 H-Cl-O |
有Fe2+、NO—3、Fe3+、NH+4、H2O和H+六种微粒,分别属于一个氧化还原反应中的反应物和生成物,下列叙述错误的是()
| A.氧化剂与还原剂的物质的量之比为8:l |
| B.若有l mol NO—3参加还原反应,则转移8mol e- |
| C.还原产物为NH+4 |
| D.若把该反应设计为原电池,则负极反应为Fe2+—e—=Fe3+ |
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用不相同的是()
| A.2Na2O2+2H2O=4NaOH+O2↑ | B.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| C.Cl2+H2O=HCl+HClO | D.2Al+2NaOH+2H2O=2NaAlO2+3H2↑ |
在 反应中,说法正确的是()
反应中,说法正确的是()
| A.Cu2O在反应中被氧化 | B.Cu2S在反应中既是氧化剂又是还原剂 |
| C.Cu既是氧化产物又是还原产物 | D.若反应中转移12mol电子,则生成6molCu |
下列推断合理的是 ()
| A.在常温下,Na2SiO3+H2O+CO2=Na2CO3+H2SiO3↓,说明H2CO3酸性强于H2SiO3; 在高温下,Na2CO3+SiO2= Na2SiO3+CO2↑,说明H2SiO3酸性强于H2CO3; |
| B.胶体区别于其他分散系的本质特点是能产生丁达尔现象 |
| C.KAl(SO4)2·12H2O是复盐;(NH4)2Fe(SO4)2也是复盐 |
| D.CaCl2、NaOH、HCl、HD四种物质都属于化合物 |
物质在反应中可表现氧化性、还原性、酸性、碱性等,下面反应的划线物质中,能在同一反应中同时表现上述两种或两种以上性质的有()
①3FeO+10HNO3==3Fe(NO3)3+NO↑+5H2O②C+2H2SO4(浓)==CO2↑+2SO2↑+2H2O
③8NH3+3Cl2==6NH4Cl+N2④NaH+H2O==NaOH+H2↑⑤2Na2O2+2H2O==4NaOH+O2↑
| A.仅有①② | B.仅有①③④⑤ | C.仅有①③⑤ | D.全部 |