同温度下,体积均为1L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g) 2NH3(g) △H=-92.6kJ/mol.测得数据如表
2NH3(g) △H=-92.6kJ/mol.测得数据如表
| 容器编号 |
起始时各物质物质的量/mol |
达到平衡时体系能量的变化 |
||
| N2 |
H2 |
NH3 |
||
| (1) |
2 |
3 |
0 |
27.78kJ |
| (2) |
1.6 |
1.8 |
0.8 |
Q |
下列叙述不正确的是
A.容器(1)(2)反应达平衡时压强相等
B.容器(2)中反应开始时v(正)>v(逆)
C.容器(2)中反应达平衡时,吸收的热量Q为9.26kJ
D.若条件为“绝热恒容”,容器(1)中反应达平衡时n(NH3)<0.6mol
可逆反应2A(g)+B(g)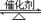 2C(g),根据下表中的数据判断下列图像错误的是()
2C(g),根据下表中的数据判断下列图像错误的是()
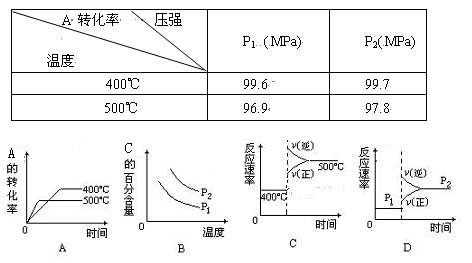
下列措施或事实能用勒沙特列原理解释的是( )
| A.在合成氨(正反应是放热)的反应中,升温有利于氨的合成 |
| B.H2、I2、HI三者的平衡混合气,加压(缩小容器体积)后颜色变深 |
| C.钢铁在潮湿的空气中更容易生锈 |
| D.氯气可以用排饱和食盐水的方法收集 |
已知“凡气体分子总数增多的反应一定是熵增大的反应”。根据所学知识判断,下列反应中,在所有温度下都不自发进行的是( )
| A.2O3(g) = 3O2(g)△H<0 | B.2CO(g) = 2C(s)+O2(g)△H>0 |
| C.N2(g) + 3H2(g) = 2NH3(g)△H<0 | D.CaCO3(s) =" CaO(s)" + CO2(g)△H>0 |
某酸碱指示剂(HIn)在水溶液中存在以下平衡:
HIn(aq)  H+ + In—(aq)
H+ + In—(aq)
(红色)(蓝色)
下列物质的溶液中,能使指示剂显蓝色的是()
| A.稀硫酸 | B.氯化铝溶液 | C.稀氨水 | D.饱和食盐水 |
下列溶液一定呈中性的是()
| A.使石蕊试液呈紫色的溶液 | B.c(H+)=c(OH-)=10-6mol/L溶液 |
| C.pH=7的溶液 | D.酸与碱恰好完全反应生成正盐的溶液 |