(12分) NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:2NaNO2+4HI===2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是________。
(2)根据上述反应,鉴别NaNO2和NaCl。可选用的物质有:①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有________(填序号)。
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是________(填编号)。
| A.NaCl | B.NH4Cl | C.HNO3 | D.浓H2SO4 |
(4)请配平以下化学方程式:
Al+ NaNO3+ NaOH=== NaAlO2+ N2↑+ H2O。若反应过程中转移5 mol e-,则生成标准状况下N2的体积为________L。
(5)在微生物的作用下, NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下: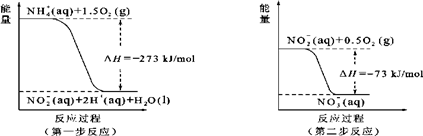
1mol NH4+(aq)全部氧化成NO3-(aq)的热化学方程式是 。
有机物A可视为是烃B分子中的所有氢原子被烃C分子中最简单的烃基取代而得到的。且已知:
①A遇Br2的CCl4溶液不褪色,其一氯代物只有一种。
②一定量的B完全燃烧,产物中n(CO2):n(H2O)=2:1,且26<M(B)<78。
③烃C为饱和链烃,通常情况下呈气态,其同分异构体不超过2种,而二溴代物有3种。
试回答下列问题:
(1)烃B的分子式为___________,若B能使酸性KMnO4溶液褪色,且所含官能团不同,则B的结构简式为。
(2)烃C的3种二溴代物的结构简式为:,,。
(3)A的分子式为。
现有A、B、C、D、E、F六种短周期元素,原子序数依次增大。已知A与D、C与E分别同主族,D、E、F同周期;A、B的最外层电子数之和与C的最外层电子数相等,A与C形成的化合物常温下均为液态,A分别与E、F形成的气体分子电子总数相等。
请回答下列问题:
(1)元素B在周期表中的位置是___________,元素D的原子结构示意图为___________。
(2)A、D、E 3种元素形成一种离子化合物,其水溶液呈碱性,试用离子方程式表示该溶液中存在的所有平衡。
(3)A2C比A2E沸点高的原因是。
(4)在一定条件下,A、C的单质和A、C、D形成的离子化合物的水溶液可构成电池,该电池正极的电极反应式为,负极的电极反应式为;
(5)该电池在放电过程中,电解质溶液的pH将_________(填“增大”、“减小”或“不变”)。
化合物B2A4 和B2C4 的液体曾被用作火箭推进剂,燃烧反应的生成物是一种气态单质和一种化合物,它们对环境无污染。1 mol B2A4与B2C4完全反应生成两种气体时放出热量516.8 kJ,则该反应的热化学方程式为。
(10分)如图所示,常温,U形管内盛有100mL的溶液,请按要求回答下列问题。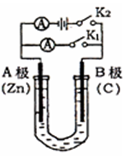
(1)若所盛溶液为CuSO4溶液,打开K2,闭合K1,则:
A为极(填“正、负”),B极的电极反应式为。
(2)若所盛溶液为滴有酚酞的NaCl溶液,打开K1,闭合K2,则:
①A电极可观察到的现象是
②总反应的化学方程式是
③反应一段时间后打开K2 ,若忽略溶液的体积变化和气体
的溶解,B极产生气体的体积(折算成标准状况)为11.2mL,
将溶液充分混合,溶液的C(OH-)为
(1)AgNO3的水溶液呈(填“酸”、“中”、“碱”)性,常温时的pH7(填“>”、“=”、“<”),原因是(用离子方程式表示):。实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以(填“促进”、“抑制”)其水解。
(2)氯化铝水溶液呈(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示)___。把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是。
(8分)炒过菜的铁锅未及时洗净,在空气中不久便会因腐蚀而出现红褐色锈斑。请回答:
(1)铁锅的锈蚀是腐蚀(填“析氢"或“吸氧” )
(2)写出铁锅腐蚀时负极的电极反应式:
(3)写出铁锅在中性条件下正极的电极反应式
(4)写出电化学反应的总方程式