对于反应N2O4⇌2NO2在温度一定时,平衡体系中NO2的体积分数V(NO2)%随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点)。下列说法正确的是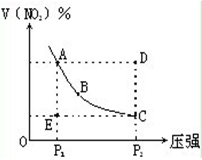
A、A、C两点的正反应速率的关系A>C
B、A、B、C、D、E各状态,V正<V逆的是状态E
C、维持P1不变,E→A所需时间为x,维持P2不变,D→C所需时间为y,则x<y
D、使E状态从水平方向到达C状态,从理论上来讲,可选用的条件是从P1突然加压至P2
亚氨基锂(Li2NH)是一种储氢容量器,安全性好的固体储氢材料,其储氢原理可表示为Li2NH+H2=LiNH2+LiH。下列有关说法正确的是
| A.Li2NH中N的化合价是-1 | B.该反应中H2既是氧化剂又是还原剂 |
| C.Li+和H+的离子半径相等 | D.此法储氢和钢瓶储氢的原理相同 |
用下图所示装置进行下列实验,实验结果与预测的现象不一致的是
| ①中的物质 |
②中的物质 |
预测①的现象 |
|
| A |
淀粉KI溶液 |
浓硝酸 |
无明显变化 |
| B |
酚酞溶液 |
浓盐酸 |
无明显变化 |
| C |
AlCl3溶液 |
浓氨水 |
有白色沉淀 |
| D |
湿润红纸条 |
饱和氯水 |
红纸条褪色] |
常温下,下列各组离子在指定溶液中能大量共存的是
| A.甲基橙呈红色的溶液:NH4+、Ba2+、AlO2-、Cl- |
| B.遇苯酚显紫色的溶液:I-、K+、SCN-、Mg2+ |
| C.与铝反应产生大量氢气的溶液:NH4+、Na+、CO32-、NO3- |
| D.加入NaOH后加热既有气体放出又有沉淀生成的溶液:Ca2+、HCO3-、NH4+、CH3COO-- |
下列说法正确的是
| A.氢键、分子间作用力、离子键、共价键都是微粒间的作用力。其中分子间作用力只影响物质的熔沸点而不影响物质的溶解性。 |
| B.石墨烯是一种从石墨材料中用“撕裂”方法剥离出的单层碳原子面材料,用这种方法从C60、金刚石等中获得“只有一层碳原子厚的碳薄片”也必将成为研究方向。 |
| C.H、S、O三种元素组成的物质的水溶液与Na、S、O三种元素组成的物质的水溶液混合可能会观察到浑浊现象。 |
D.原子结构模型的演变经历了: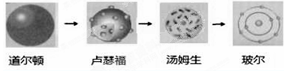 |
下列表示物质结构的化学用语或模型图正确的是
A.H2O2的电子式: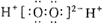 |
B.O2-的结构示意图: |
| C.二氧化硅的分子式:SiO2 |
D.质子数为8,中子数为10的氧原子: |