将一定量铁粉和铜粉的混合物加入由稀硫酸和稀硝酸组成的混合溶液中,充分反应后金属粉末有剩余,下列有关推断正确的是
| A.反应过程中不可能产生H2 |
| B.往反应后的溶液中加入KSCN溶液会变血红色 |
| C.剩余的金属粉末中一定有铜 |
| D.往反应后的溶液中加入足量的稀H2SO4,则金属粉末的质量一定会减少 |
氢氧燃料电池以氢气作还原剂,氧气作氧化剂,电极为多孔镍,电解质溶液为30%的氢氧化钾溶液。下列说法正确的是:
| A.负极反应为:2H2+4OH- - 4e- = 4H2O |
| B.负极反应为:O2+2H2O+4e-= 4OH- |
| C.电池工作时溶液中的阴离子移向正极移动 |
| D.电池工作时正极区pH升高,负极区pH下降 |
下列关于0.1 mol·L-1 NH4Cl溶液的说法正确的是
| A.向溶液中加滴加几滴浓盐酸,c(NH4+)减少 |
| B.向溶液中加入少量CH3COONa固体,c(NH4+)减少 |
| C.溶液中离子浓度关系为:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D.向溶液中加适量氨水使混合液的pH=7,混合液中c(NH4+)>c(Cl-) |
下列实验装置设计正确,且能达到目的的是
短周期非金属元素甲~戊在元素周期表中的相对位置如右表所示,下面判断正确的是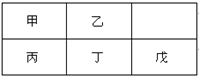
| A.原子半径:甲<乙 |
| B.非金属性:乙<丁 |
| C.最高价氧化物的水化物的酸性:丙<丁 |
| D.最外层电子数:丙>丁>戊 |
下列说法中正确的是
| A.乙醇与乙酸都存在碳氧双键 |
| B.油脂水解可得到氨基酸和甘油 |
| C.淀粉和纤维素水解最终产物都是葡萄糖 |
| D.卤代烃加入硝酸酸化的硝酸银溶液可根据生成的卤化银沉淀颜色检验卤原子 |