下列离子方程式或化学反应方程式与所述事实相符且正确的是
A.将2molSO3气体通入一密闭容器中,反应达平衡后吸收QkJ热量,则该反应的热化学方程式为:2SO3(g) 2SO2(g)+O2(g) △H=" +Q" kJ/mol 2SO2(g)+O2(g) △H=" +Q" kJ/mol |
| B.向20mL0.5mol·L-1FeBr2溶液中通入224mL Cl2(标准状况):2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
| C.以金属银为阳极电解饱和硫酸铜溶液 Cu2+ + 2H2O=" 2Cu" + O2↑+ 4H+ |
| D.NH4Al(SO4)2溶液中加入Ba(OH)2溶液至恰好使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
PCl5(气)  PCl3(气) +Cl2(气) △H>0 当反应达到平衡时,下列措施:①降温②恒容通入惰性气体③增加Cl2的浓度④加压⑤加催化剂⑥恒压通入惰性气体,能提高PCl5质量分数的是
PCl3(气) +Cl2(气) △H>0 当反应达到平衡时,下列措施:①降温②恒容通入惰性气体③增加Cl2的浓度④加压⑤加催化剂⑥恒压通入惰性气体,能提高PCl5质量分数的是
| A.①②④ | B.①③④ | C.②③⑥ | D.③⑤⑥ |
下列电离方程式书写正确的是()
A.Ca(OH)2 Ca2++ 2OH- Ca2++ 2OH- |
B.H2SO3 2H++ SO32- 2H++ SO32- |
C.NaHS  Na++ HS- Na++ HS- |
D.HCO3— H++ CO32- H++ CO32- |
已知汽车尾气无害化处理反应为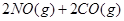

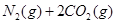 下列说法不正确的是
下列说法不正确的是
| A.反应达到平衡后,N0的反应速率保持恒定 |
| B.使用高效催化剂可有效提高正反应速率 |
| C.升高温度可使该反应的逆反应速率降低 |
| D.单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡 |
已知反应mA(g)+nB(g)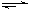 y C(g),如图表示在不同条件下反应物B的体积分数φ(B)随时间变化的关系,据此判断
y C(g),如图表示在不同条件下反应物B的体积分数φ(B)随时间变化的关系,据此判断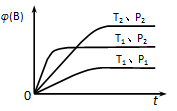
A.m+m<y ,△ H<0
B.m+m>y ,△ H>0
C.m+m<y ,△ H>0
D.m+m>y ,△ H<0
盖斯定律在生产和科学研究中有很重要的作用,有些反应的反应热虽然无法直接测得,但可以利用盖斯定律间接计算求得。已知7.2 g碳在12.8g的氧气中燃烧,至反应物耗尽,放出x kJ热量。已知单质碳的燃烧热为y 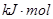
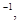 则1 mol C与
则1 mol C与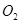 反应生成CO的反应热
反应生成CO的反应热 H为
H为
A.-(2.5x -0.5 y)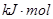 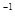 |
B.-(5x - 0.5y) 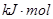 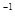 |
C.-(10x - y)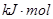 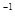 |
D.- y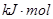 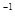 |