(本题8分)对于反应xA(g)+yB(g)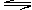 pC(g)+qD(g)压强与温度对C的质量分数的影响如图:
pC(g)+qD(g)压强与温度对C的质量分数的影响如图: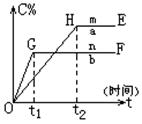
(1)若m、n表示不同温度,则m n,正反应为 反应(填“放热”、“吸热”);
(2)若m、n表示不同压强,则m n,(x+y) (p+q)(填<、>、=);
(3)b曲线的OG段比a曲线的OH段陡的原是: ;
(4)a曲线的HE段高于b曲线的GF段的原是: 。
酿酒和造醋是古代劳动人民的智慧结晶,白酒和醋也是日常生活中常见的有机物。
(1)醋酸可用于除去水壶中的水垢,成份主要是CaCO3和Mg(OH) 2。写出醋酸与Mg(OH) 2反应的离子方程式_______________________。食盐中常加入KIO3来补碘,为验证食盐中的KIO3,可在食盐中加入醋酸,再加入KI和淀粉溶液。反应的离子方程式为____________________________。
(2)酿制米酒的过程中是米中的淀粉在酶的作用下生成葡萄糖。写出化学方程式_____________________________,然后葡萄糖在酶的作用下生成乙醇。
(3)在酿制米酒的过程中,有可能变酸,这里因为产生了醋酸。为了除去米酒中的酸味有人建议向米酒中加入红热的铅,使它与醋酸生成有甜味的醋酸铅。你认为此法是否可行_____(填行,不可行),原因是___________________________________。
有机物A(分子式C6H10O3)是合成某种隐形眼镜材料的单体,A可发生如下变化:
已知:Ⅰ.物质B是最简单的二元醇,可用作汽车发动机抗冻剂;物质D不能发生银镜反应,但能与NaHCO3溶液反应放出气体。
Ⅱ.
回答下列问题:
(1)隐形眼镜材料的结构简式为;
(2)B可由最简单的烯烃和某常见无机物在一定条件下经一步反应合成,则该无机物的电子式为:;
写出物质B在铜催化下与O2反应的化学方程式。
(3)写出与C具有完全相同官能团的C的同分异构体的结构简式(不包含C):
。
(4)可用下图所示方法由物质D制取乙二酸:
则合成路线中I的结构简式为:;反应条件II为:。
A为药用有机物,A存在如下图所示的转化关系。已知A在一定条件下能跟醇发生酯化反应,A分子中苯环上的两个取代基处于邻位,D能跟NaOH 溶液反应。
请回答:
(1)A转化为B、C时,涉及到的反应类型有、。
(2)E的两种同分异构体Q、R都能在一定条件下发生银镜反应,R能与Na反应放出H2,而Q不能。Q、R的结构简式为Q、R。
(3)D的结构简式为。
(4)写出A在加热条件下与 溶液反应的化学方程式。
溶液反应的化学方程式。
(5)已知: ,且苯酚和乙酸在一定条件下能发生酯化反应。请选用适当物质设计一种合成方法,用邻甲基苯酚经两步反应合成有机物A,在方框中填写有机物的结构简式。
,且苯酚和乙酸在一定条件下能发生酯化反应。请选用适当物质设计一种合成方法,用邻甲基苯酚经两步反应合成有机物A,在方框中填写有机物的结构简式。
有机物A(C11H12O2)可调配果味香精。可用含碳、氢、氧三种元素的有机物B和C为原料合成A。
(1)B的蒸汽密度是同温同压下氢气密度的23倍,分子中碳、氢原子个数比为1:3。有机物B的分子式为。
(2)有机物C的分子式为C7H8O,C能与钠反应,不与氢氧化钠溶液反应,也不能使溴的四氯化碳溶液褪色。C的结构简式为,C与苯酚是否互为同系物: (填“是”或“否”)
(3)已知两个醛分子间能发生如下反应: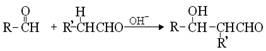 (﹣R、﹣R’表示氢原子或烃基)
(﹣R、﹣R’表示氢原子或烃基)
用B和C为原料按如下路线合成A:
①上述合成过程中涉及到的反应类型有:(填写序号)
a取代反应;b 加成反应;c 消去反应;d 氧化反应;
②写出D与银氨溶液反应的化学方程式:。
③ F的结构简式为:。
④写出G和B反应生成A的化学方程式:。
(4)F的同分异构体有多种,写出既能发生银镜反应又能发生水解反应,且苯环上只有一个取代基的所有同分异构体的结构简式。
(10分)已知有机物A的结构简式为: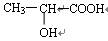 ,回答下列问题:
,回答下列问题:
(1)A中所含官能团的名称为:;
下列各物质分别与A以任意比混合,若只要总物质的量不变,则消耗氧气的量也不变的是(填字母代号)
| A.C2H6O | B.C3H4O2 | C.C2H4 | D.C3H6 |
(2)在一定条件下,A能反应生成一种六元环酯,该反应的化学方程式为:
(3)在一定条件下,A还能反应生成一种高分子化合物,该反应的化学方程式为:
(4)在一定条件下,A能反应生成B,B能使溴的四氯化碳溶液褪色,B还能反应生成高分子化合物C,请写出由B生成C的化学方程式: