烧碱、纯碱等都是重要的化工原料。
(1)利用如图装置可以证明二氧化碳与烧碱溶液发生了反应。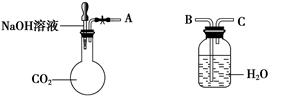
①若将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是____________。
②若其他操作不变,将A与C连接,可观察到的现象是_____________________。
(2)向100 mL 1 mol·L-1烧碱溶液中通入一定量CO2充分反应后,将溶液在低温下蒸干得到白色固体X,X的组成可能有四种情况,按出现的先后顺序分别是Ⅰ.NaOH、Na2CO3,Ⅱ.__________________,Ⅲ.Na2CO3、NaHCO3,Ⅳ.__________________。
①常温下,将得到的固体X重新溶于水,在所得溶液中逐滴加入盐酸,得到下面的变化图,则X的成份为 (填Ⅰ、Ⅱ、Ⅲ或Ⅳ),盐酸的浓度为 。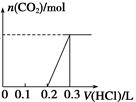
②若要验证白色固体X是第Ⅰ种组成,依次加入的试剂为________(填字母序号)。
a.盐酸 b.MgCl2溶液 c.BaCl2溶液 d.Ba(OH)2溶液
在验证的过程中,一定需要进行的操作是________(填字母序号)。
a.萃取 b.洗涤 c.过滤 d.分馏
③若白色固体X为第Ⅲ种组成,下列实验方案中不能测定其中NaHCO3质量分数的是________(填字母序号)。
a.取m g X与足量Ba(OH)2溶液充分反应,过滤,洗涤,烘干得n g固体
b.取m g X与足量盐酸充分反应,加热,蒸干,灼烧得n g固体
c.取m g X充分加热,减重n g
d.取m g X与足量稀硫酸充分反应,逸出的气体被足量碱石灰吸收,增重n g
④若白色固体X的质量为5.0 g,则X的组成为________(填Ⅰ、Ⅱ、Ⅲ或Ⅳ)。
氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
(1)氢氧燃料电池的能量转化主要形式是由转化为,在导线中电流方向为→(用a、b 表示)。
(2)正极反应式为,负极发生反应(填“氧化”或“还原”)。
(3)氢氧燃料电池的能量转化率100%(填<、>、=)。
(4)电极表面镀铂粉的原因为。
肉桂醛(C9H8O)是一种常用香精,在食品、医药化工等方面都有应用。肉桂醛与其他有机物具有如下转化关系,其中A为一氯代烃。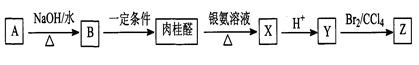
(1)肉桂醛是苯的一取代物,与H2加成的产物中没有支链,肉桂醛结构简式是。
(2)反应A→B的化学方程式是________________________________。
(3)Z不能发生的反应类型是(填字母)___________。
a. 取代反应 b. 加聚反应 c. 加成反应 d. 消去反应
(4)Y与乙醇在一定条件下反应的化学方程式是:____________________。
(5)写出符合下列条件的Y的一种同分异构体的结构:______________________________。
①属于酯类②苯环上只有一个取代基③能发生银镜反应。
医药阿斯匹林的结构简式如下,试根据阿斯匹林的结构回答: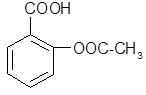
⑴阿斯匹林看成酯类物质,口服后,在胃肠酶的作用下,阿斯匹林发生水解反应,生成A和B 两种物质。其中A的结构简式为 ,则B的结构简式为;B中含有的官能团是。
,则B的结构简式为;B中含有的官能团是。
⑵阿斯匹林跟小苏打同时服用,可使上述水解产物A与小苏打反应,生成可溶性盐随尿液排出,该反应的化学方程式为:。
⑶上述水解产物A与氢氧化钠溶液反应的化学方程式为;
⑷上述水解产物B与乙醇、浓硫酸共热反应的化学方程式为:;
本题包括A、B两小题,请选定其中一小题并在相应的答
题区域内作答。若多做,则按A小题评分。
A.【物质结构与性质】
元素H、C、N、O、F都是重要的非金属元素,Fe、Cu是应用非常广泛的金属。
(1)Fe元素基态原子的核外电子排布式为。
(2)C、H元素形成的化合物分子中共有16个电子,该分子中 键与
键与 键的个数比为
键的个数比为
。
(3)C、N、O三种元素的第一电离能由大到小的顺序为(用元素符号表示)
。
(4)在测定HF的相对分子质量时,实验测得值一般高于理论值,其主要原因是
。
(5)C、N两元素形成的化合物 形成的原子晶体,结构类似
形成的原子晶体,结构类似
金刚石,甚至硬度超过金刚石,其原因是。
(6)右图为石墨晶胞结构示意图,该晶胞中含有C原子的个数为。
B.【有机化学基础】
扑热息痛(学名对乙酸氨基酚)是生活中常用到的一种解热镇痛药。以苯为原料合成扑热息
痛的部分转化如下:
请回答下列问题:
(1)B C的反应类型为,D中官能团的名称为。
C的反应类型为,D中官能团的名称为。
(2)C的结构简式为。
(3)1mol扑热息痛与足量 溶液反应,理论上消耗
溶液反应,理论上消耗 的物质的量为mol。
的物质的量为mol。
(4)实验证明B能够与溴水反应,试写出其反应的化学方程式。
(5)扑热息痛有多种同分异构体,同时符合下列要求的同分异构体有种。
①苯环上有两个对位取代基;②同于氨基酸。
甲醇( )是重要的能源物质,研究甲醇具有重要意义。
)是重要的能源物质,研究甲醇具有重要意义。
(1)利用工业废气中的 可制取甲醇,其反应为:
可制取甲醇,其反应为:
常温常压下已知下列反应的能量变化如图所示:
写出由二氧化碳和氢气制备甲醇的热化学方程式:
。
(2)为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了 的
的  晶体,在高温下它能传导
晶体,在高温下它能传导 离子。电池工作时正极反应为。
离子。电池工作时正极反应为。
若以该电池为电源,用石墨做电极电解100mL含有如下离子的溶液。
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的物质的量为mol。
(3)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后将 氧化成
氧化成 ,然后以
,然后以 做氧化剂把水中的甲醇氧化成
做氧化剂把水中的甲醇氧化成 而净化。实验室用下图装置模拟上述过程:
而净化。实验室用下图装置模拟上述过程:
①写出阳极电极反应式;
②除去甲醇的离子反应为:
 ,该过程中被氧化的元素是 ,当产生标准状况下2.24L
,该过程中被氧化的元素是 ,当产生标准状况下2.24L 时,共转移电子mol。
时,共转移电子mol。