下列指定反应的离子方程式,正确的是
| A.氢氧化亚铁溶于稀硝酸中:Fe (OH)2+2H+=Fe2++2H2O |
| B.碳酸钙溶于稀醋酸溶液:CaCO3+ 2H+=Ca2+ + CO2↑+ H2O |
| C.向NH4Al (SO4)2溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀:2Ba2++4OH-+Al3++2SO42-=2BaSO4↓+AlO2-+2H2O |
| D.向苯酚钠溶液中通入少量的CO2:C6H5O-+CO2+H2O → C6H5OH+HCO3- |
下列有关实验中,叙述正确的是
| A.用KMnO4溶液洗气可除去CO2中的SO2 |
| B.用玻璃棒搅拌漏斗中的液体以加快过滤的速度 |
| C.用pH 试纸测溶液pH时,需先用蒸馏水润湿试纸 |
| D.浓硫酸与水混合时,将水慢慢倒入浓硫酸中,边加边搅拌 |
有①氨水 ②NH4Cl溶液 ③Na2CO3溶液 ④NaHCO3溶液各25 mL,物质的量浓度均
为0.1 mol·L-1,下列说法正确的是
| A.4种溶液pH的大小顺序:①>④>③>② |
| B.溶液①、②等体积混合后pH > 7,则c(NH4+) < c(NH3·H2O) |
| C.向溶液③、④中分别加入12.5 mL 0.1 mol·L-1 NaOH溶液后,两溶液中的离子种类相同 |
| D.向溶液①、②中分别加入25 mL 0.1 mol·L-1盐酸后,溶液中c(NH4+):①>② |
用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.1 mol Cl2与足量的铁反应,转移的电子数为3NA |
| B.在含Al3+总数为NA的AlCl3溶液中,Cl—总数为3NA |
| C.将pH=2的盐酸和pH=4的硫酸等体积混合,所得溶液pH=3 |
| D.标准状况下,l mol SO3含有的氧原子数为3NA |
下列说法错误的是
| A.0.1 mol·L-1的CH3COOH溶液中,由水电离的c(H+)为10-13 mol·L-1 |
| B.pH=2与pH=1的CH3COOH溶液中c(H+)之比为1︰10 |
| C.等体积pH=12的NaOH溶液和pH=2的CH3COOH溶液混合,混合后溶液pH<7 |
| D.1.0 mol·L-1Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
某原电池装置如下图所示。下列有关叙述中,正确的是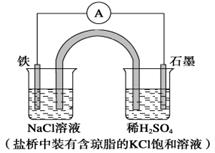
| A.Fe作正极,发生氧化反应 |
| B.负极反应:2H++2e-===H2↑ |
| C.工作一段时间后,两烧杯中溶液pH均不变 |
| D.工作一段时间后,NaCl溶液中c(Cl-)增大 |