(12分)硫酸锌是制备荧光粉的原料之一。工业上由锌白矿(主要成分是ZnO,还含有Fe2O3、CuO、SiO2等杂质)制备ZnSO4•7H2O的流程如下:
已知:常温下,溶液中的Fe3+、Zn2+、Fe2+以氢氧化物形式开始沉淀的pH分别为:2.7,5.4,7.6;完全沉淀的pH分别为:3.7,6.5,9.7。
(1)下列能提高浸取过程中浸出效率的措施有
| A.将矿石粉碎 | B.提高浸取温度 | C.适当增加硫酸的浓度 | D.搅拌并适当延长浸取时间 |
ZnO和硫酸反应的离子方程式为
(2)加入适量锌粉后溶液中存在的金属阳离子主要有
(3)氧化过程中H2O2发生反应的化学方程式为
(4)加入适量Ca(OH)2调节溶液pH至 ~ (填范围),促进Fe3+水解完全。Fe3+水解反应的平衡常数表达式K=
.有机化学反应因反应条件不同,可生成不同的有机产品。例如:
(一)苯的同系物与卤素单质混合,在光照条件下,侧链上的氢原子被卤素原子取代;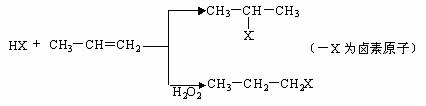
(二)工业上利用上述信息,按下列路线合成结构简式为的物质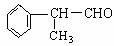 ,该物质是氢化阿托醛一种香料。
,该物质是氢化阿托醛一种香料。
请根据上述路线,回答下列问题:
(1)A为一氯代物,它的结构简式可能为_______________________________________。
(2)工业生产过程中,中间产物必须经过②③④得到D,而不采取直接转化为D的方法原因是_____________________________________。
(3)写出反应类型②_________、③_________。
(4)反应④的化学方程式为:__________________________________________。
(5)氢化阿托醛与氢气1:1加成后的产物C9H10O的同分异构体很多,写出两种符合下列三个条件的 C9H10O的同分异构体的结构简式:__________________、___________________。
①能与溴水反应
②能与氢氧化钠溶液反应
③分子中只有苯环一种环状结构,苯环上有两个取代基,且苯环上的一溴代物有两种;
(6)氢化阿托醛发生银镜反应的化学方程式为_____________________________________。
(12分)据《中国制药》报道,化合物F是用于制备“非典”药品(盐酸祛炎痛)的中间产物,其合成路线为:
已知:(Ⅰ)RNH2+R/CH2Cl  RNHCH2 R/+HCl(R和R/代表烃基)
RNHCH2 R/+HCl(R和R/代表烃基)
(Ⅱ)苯的同系物能被酸性高锰酸钾溶液氧化,如:
(Ⅲ)
(苯胺,弱碱性,易氧化)
(Ⅳ) 与浓硫酸、浓硝酸混合在不同温度下会得到不同产物。
与浓硫酸、浓硝酸混合在不同温度下会得到不同产物。
回答下列问题:
(1)反应①的条件是_______________________________
(2)反应③和反应④的顺序不能颠倒,原因是_____________________________________
(3)C的结构简式是_________________。
(4)D+E→F的化学方程式:_____________________。
(5)反应①~⑤中,属于取代反应的是(填反应序号)_______________ 。
.奶油中有一种只含C、H、O的化合物A。A可用作香料,其相对分子质量为88,分子中C、H、O原子个数比为2:4:1。
(1)A的分子式为______________。
(2)写出与A分子式相同的酯的同分异构体有________________种。
已知:①A中含有碳氧双键,A既不是羧酸也不是酯
②G的一氯代物只有一种
③
 RCHO+R´CHO
RCHO+R´CHO
与A相关的反应如下:
(3)A中含有的官能团为_____________________
(4)写出A→G、B→D的反应类型分别为: ____________、 ______________。
(5)写出A、C、G的结构简式:A________________________、C_______________________、F____________________。
(6)写出E→F反应的化学方程式_____________________________________________。
. 已知:A、B、C、D均为芳香族化合物,且式量B>A>C,已知有机物A的结构简式为:
(1) A既能与NaOH溶液反应,又能与NaHCO3溶液反应,1mol A和过量NaHCO3溶液反应生成CO2_________mol。
(2) 有机物B在浓H2SO4存在条件下,相互作用生成一种环状酯如图。写出B的结构简式_________________。
等物质的量B与Na、NaOH、NaHCO3充分反应,消耗Na、NaOH、NaHCO3的物质的量之比为_______________________。
(3) 1molA、C完全燃烧,消耗氧气的质量相等,且1molC能和1molNa完全反应,写出含碳原子数最少的C的结构简式为_____________________________。
A~G都是有机化合物,它们的转化关系如下:
请回答下列问题:
(1)已知:6.0g化合物E完全燃烧生成8.8gCO2和3.6gH2O;E的蒸气与氢气的相对密度为30,则E的分子式为_______________:
(2)A为一取代芳烃,B中含有一个甲基。由B生成C的化学方程式;
(3)由B生成D、由C生成D的反应条件分别是_______________、_____________;
(4)由A生成B、由D生成G的反应类型分别是_______________、_____________;
(5)F存在于栀子香油中,其结构简式为_______________;
(6)在G的同分异构体中,苯环上一硝化的产物只有一种的共有________个,分子中有两种不同化学环境的氢原子且两种氢原子数目相等的是(填结构简式)。