纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是 。
(2)已知:①2Cu(s)+1/2O2(g)=Cu2O(s) △H = -akJ·mol-1
②C(s)+1/2O2(g)=CO(g) △H = -bkJ·mol-1
③Cu(s)+1/2O2(g)=CuO(s) △H = -ckJ·mol-1
则方法Ⅰ发生的反应:2CuO(s)+C(s)= Cu2O(s)+CO(g) △H = kJ·mol-1。
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极反应式为 。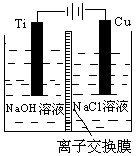
(4)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2。该制法的化学方程式为 。已知肼与氨相似,则它与足量盐酸反应的方程式
(5)在相同的密闭容器中,用以上两种方法制得的Cu2O分别进行催化分解水的实验:
2H2O(g)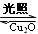 2H2(g)+ O2(g)△H>0 水蒸气的浓度随时间t变化如下表所示。
2H2(g)+ O2(g)△H>0 水蒸气的浓度随时间t变化如下表所示。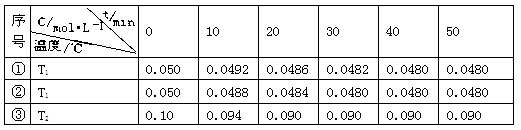
下列叙述正确的是 (填字母代号)。
A.实验的温度:T2<T1
B.实验①前20 min的平均反应速率 v(O2)=7×10-5 mol·L-1 min-1
C.实验②比实验①所用的催化剂催化效率高
有原子序数依次增大的A、B、C、D、E、F六种短周期元素;A元素的原子半径是所有元素中原子最小的;C元素的最高价氧化物对应水化物与其氢化物能生成盐M;E与A同主族,且与E同周期;F元素原子的最外层电子数比次外层电子数少2;A、B、C、E、F这五种元素,每—种与D元素都能形成原子个数比不相同的若干种化合物。请回答:
(1)D元素在周期表中的位置为______________。
(2)可以比较D和F得电子能力强弱的是___________________(填写编号)。
a.比较这两种元素原子半径的大小
b.二者形成的化合物中,D元素的原子显负价
c.比较这两种元素的气态氢化物的稳定性
(3)盐M中含有的化学键类型有______________________;并写出其中阳离子的电子式_________________。
(4)已知1molE与水反应放出283.5kJ的热量,试写出E与水反应的热化学反应方程式
________________________________________________________________。
(5)固体氧化物燃料电池(SOFC)以固体氧化物作为电解质。其工作原理如下图所示。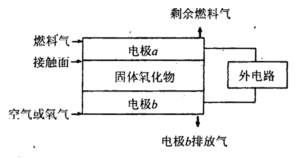
①固体氧化物中的O2-向_________(填“正”或“负”)极移动。
②电极b为电池_________极,其电极反应式为______________________________。
③若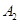 作为燃料气,则接触面上发生的反应为______________________________。
作为燃料气,则接触面上发生的反应为______________________________。
④若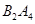 作为燃料气,则接触面上发生的反应为________________________________。
作为燃料气,则接触面上发生的反应为________________________________。
有机物A是一种军用催泪弹的主要有效成分。经分析A的相对分子质量为161,除含有C、H元素外,它还含有一种卤族元素,且分子中只含有一个甲基。化合物A~F的转化关系如下图所示,其中足量的新制Cu(OH)2悬浊液与1mol C反应可生成1mol Cu2O 和1mol D,B1和B2均为较稳定的化合物且互为同分异构体。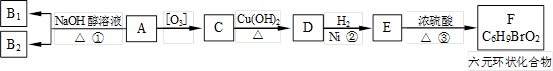
已知:①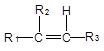
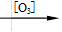
 +
+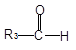
②一个碳原子上连有两个碳碳双键的结构(—C=C=C—)不稳定。
请完成下列问题;
(1)化合物A含有的官能团是。B1的相对分子质量是。
(2)①、②、③的反应类型分别是。
(3)写出A、F的结构简式:
A.;F.。
(4)写出C→D反应的化学方程式:
。
(5)符合下列条件的C的同分异构体共有________种。
①含有二个甲基;②含有二个醛基。
2004年诺贝尔化学奖授予阿龙·切哈诺沃等三位科学家,以表彰他们发现了泛素调节的蛋白质降解。化合物A是天然蛋白质水解的最终产物,其相对分子质量为165,其中O元素的质量分数小于20%,N元素的质量分数小于10%。
(1)化合物A的分子式为;光谱测定显示,化合物A分子结构中不存在甲基(—CH3),则化合物A的结构简式为。写出A发生缩聚反应的方程式
。
(2)化合物B是A的同分异构体,是某芳香烃一硝化后的唯一产物(硝基连在芳环上)。则化合物B的结构简式是。
写出制备TNT的化学方程式。
重晶石矿(主要成分为硫酸钡)因为含有Fe2O3、MnO及炭质等杂质而常呈深褐色。工业上将重晶石矿粉碎后与硫酸、铝粉在反应槽中混合加热(即“漂白”),再经水洗等一系列工序制得白色的重晶石填料,广泛用作纸张、油漆等的填充剂。已知MnO是碱性氧化物,Al粉可以将深色的Fe3+转化为浅色的Fe2+。
重晶石填料的生产工艺流程为:
(1)在该流程中,为加快“漂白”速度,采取的措施有、
。
(2)硫酸起到了“漂白”的作用。请写出硫酸直接起到该作用时的化学方程式:
、。
(3)二次漂白水洗过滤后,检验滤渣不含Fe2+离子的方法是
、。
(4)二次漂白前,煅烧的主要目的是。将煅烧后的固体磨成细粉,使用的是加有刚玉球的振动磨。这说明刚玉具有很高的。
(5)工业生产中为了充分利用资源,将滤液经过处理得到化工原料Fe2O3。操作过程是:
①滤液中通入过量Cl2,其目的是。
②再加入适量NaOH来调节溶液的pH ,其目的是,调节溶液的pH范围为。
有关离子开始沉淀及完全沉淀时的pH如下:
| 离子 |
开始沉淀时的pH |
完全沉淀时的pH |
| Fe2+ |
7.6 |
9.7 |
| Fe3+ |
2.7 |
3.7 |
| Al3+ |
3.8 |
4.7 |
| Mn2+ |
8.3 |
9.8 |
(6)最后通过、得到氧化铁。
向某密闭容器中加入0.15mol/L A、0.05mol/L C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示[t0时c( B)未画出,t1时增大到0.05mol/L]。乙图为 t2时刻后改变反应条件,平衡体系中正、逆反应速率随时间变化的情况。
(1)若t4时改变的条件为减小压强,则B的起始物质的量浓度为mol/L;
该反应的平衡常数表达式为K=。
(2)若t5时改变的条件是升温,此时v(正) > v(逆),平衡常数K的值将(选填“增大”、“减小”或“不变”)。
(3)若 t1= 15s,则t0~ t1阶段以C 浓度变化表示的平均反应速率为v(C)=
mol/L·s。t3时改变的某一反应条件可能是(选填序号)。
a.使用催化剂 b.增大压强c.增大反应物浓度 d.降低产物浓度
(4)若A的物质的量减少0.02mol时,容器与外界的热交换总量为a kJ,写出该反应的热化学方程式。